
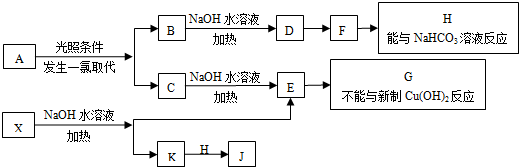
 ,B最终产物H能与NaHCO3溶液反应,说明H具有酸性,则B为
,B最终产物H能与NaHCO3溶液反应,说明H具有酸性,则B为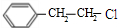 ,B发生水解反应生成D为
,B发生水解反应生成D为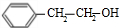 ,D发生氧化反应生成F为
,D发生氧化反应生成F为 ,F发生氧化反应生成H为
,F发生氧化反应生成H为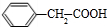 ,则C为
,则C为 ,C发生水解反应生成E为
,C发生水解反应生成E为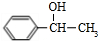 ,X分子式为C15H14O3,能使FeCl3溶液显紫色,说明结构中含有酚羟基,水解生成K和E,则X为酯,K酸化得到J,而E为醇,则J为酸,且J分子中含有酚羟基,J分子式为C7H6O3,J分子在核磁共振氢谱中有4个特征吸收峰,则J为
,X分子式为C15H14O3,能使FeCl3溶液显紫色,说明结构中含有酚羟基,水解生成K和E,则X为酯,K酸化得到J,而E为醇,则J为酸,且J分子中含有酚羟基,J分子式为C7H6O3,J分子在核磁共振氢谱中有4个特征吸收峰,则J为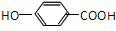 ,K为
,K为 ,X为
,X为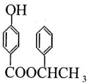 ,据此解答.
,据此解答. ,B最终产物H能与NaHCO3溶液反应,说明H具有酸性,则B为
,B最终产物H能与NaHCO3溶液反应,说明H具有酸性,则B为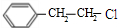 ,B发生水解反应生成D为
,B发生水解反应生成D为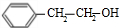 ,D发生氧化反应生成F为
,D发生氧化反应生成F为 ,F发生氧化反应生成H为
,F发生氧化反应生成H为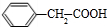 ,则C为
,则C为 ,C发生水解反应生成E为
,C发生水解反应生成E为 ,X分子式为C15H14O3,能使FeCl3溶液显紫色,说明结构中含有酚羟基,水解生成K和E,则X为酯,K酸化得到J,而E为醇,则J为酸,且J分子中含有酚羟基,J分子式为C7H6O3,J分子在核磁共振氢谱中有4个特征吸收峰,则J为
,X分子式为C15H14O3,能使FeCl3溶液显紫色,说明结构中含有酚羟基,水解生成K和E,则X为酯,K酸化得到J,而E为醇,则J为酸,且J分子中含有酚羟基,J分子式为C7H6O3,J分子在核磁共振氢谱中有4个特征吸收峰,则J为 ,K为
,K为 ,X为
,X为 ,
, ,X的结构简式为
,X的结构简式为 ,故答案为:
,故答案为: ;
; ;
; ,所含的含氧官能团的名称为:羧基、羟基,故答案为:羧基、羟基;
,所含的含氧官能团的名称为:羧基、羟基,故答案为:羧基、羟基; ,属于酯化反应(或取代反应),
,属于酯化反应(或取代反应), ,酯化反应(或取代反应);
,酯化反应(或取代反应);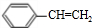 ,以I为单体合成的高分子化合物的结构简式是
,以I为单体合成的高分子化合物的结构简式是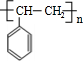 ,故答案为:
,故答案为: ;
;  )的同分异构体符合条件:
)的同分异构体符合条件: ,
, 任意一种.
任意一种.


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
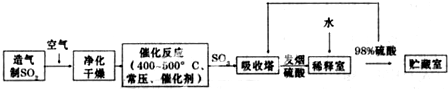
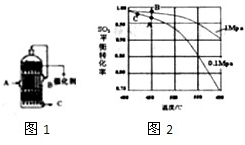
| 氧气 |
| 热空气或 |
| 水蒸气 |
| 碱液 |
| 吸收 |
| 酸化 |
| 蒸馏 |
| 煅烧 |
| 水 |
| 海水 |
| 过滤 |
| 灼烧 |
| 熔化 |
| 电解 |
| 放电 |
| 水 |
| 吸收 |
| 一定条件下 |
| 合成塔 |
| 过量氯气 |
| 水冷 |
| 分离 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)有A、B、C、D四种金属,已知:只有D投入水中可与水剧烈反应;用B和C作电极,稀硫酸作电解质溶液构成原电池时,C为正极;A和C的离子共存于电解液中,以石墨为电极电解时阴极析出A.则这四种金属的活动性由强到弱的顺序是
(1)有A、B、C、D四种金属,已知:只有D投入水中可与水剧烈反应;用B和C作电极,稀硫酸作电解质溶液构成原电池时,C为正极;A和C的离子共存于电解液中,以石墨为电极电解时阴极析出A.则这四种金属的活动性由强到弱的顺序是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
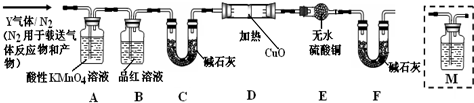
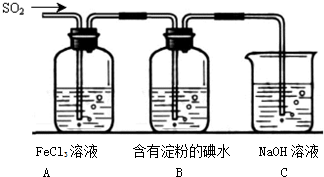
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验操作 | 实验现象或 预期实验现象 | 现象解释(用 离子方程式表示) | |
| 猜想② | 溶液pH=8 | ||
| 向pH=2的硫酸中 滴加Na2S2O3溶液 | 2S2O32-+2H+══S↓+SO2↑+H2O | ||
| 猜想③ | 向新制氯水中滴加少量Na2S2O3溶液 | 氯水颜色变浅 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、MnO4-、Cl-、Ba2+ |
| B、Na+、Ba2+、HCO3-、NO3- |
| C、K+、NO3-、CO32-、Cl- |
| D、Na+、H+、Cl-、S2- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com