
| A. | ①②⑤⑥⑦ | B. | ①②④⑤⑥ | C. | ⑤⑦ | D. | ④⑤⑦ |
分析 ①求出28g氮气的物质的量,然后根据氮气为双原子分子来分析;
②求出4g金属钙的物质的量,然后根据变成钙离子时失去2个电子来分析;
③常温常压下气体摩尔体积大于22.4L/mol;
④氖气为双原子分子;
⑤质量m=nM来计算;
⑥标准状况下水为液体,不能根据气体摩尔体积来计算;
⑦求出17g氨气的物质的量,然后根据氨气中含10个电子来分析.
解答 解:①28g氮气的物质的量为1mol,而氮气为双原子分子,故1mol氮气中含2NA个原子,故①错误;
②4g金属钙的物质的量为0.1mol,而变成钙离子时失去2个电子,故0.1mol钙失去0.2NA个电子,故②错误;
③在常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氮气的物质的量小于0.5mol,故分子个数小于0.5NA个,故③错误;
④氖气为单原子分子,故1mol氖气中含NA个原子,故④正确;
⑤0.5mol铝的质量m=0.5mol×27g/mol=13.5g,故⑤正确;
⑥标况下水为液体,不能根据气体摩尔体积来计算气物质的量和分子个数,故⑥错误;
⑦17g氨气的物质的量为1mol,而氨气中含10个电子,故1mol氨气中含10NA个电子,故⑦正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:选择题
如图锥形瓶中装满了c mol·L-1的Na2SO4溶液,经测定其中含有a mol SO42-,则锥形瓶容积为( )

A.a/c L B.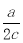 L C.ac L D.2ac L
L C.ac L D.2ac L
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
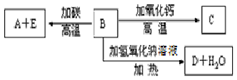 A、B、C、D、E代表单质或化合物,它们之间的相互转换关系如图所示.A为地壳中含量仅次于氧的非金属元素的单质.
A、B、C、D、E代表单质或化合物,它们之间的相互转换关系如图所示.A为地壳中含量仅次于氧的非金属元素的单质.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入盐酸酸化的BaCl2溶液,生成白色沉淀 | 该溶液中不一定含有SO42- |
| B | 光洁的铁钉放在冷的浓硫酸中,无明显现象 | 铁钉与冷的浓硫酸不反应 |
| C | 将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡静置,下层分别呈无色和紫红色 | 氧化性:Br2>Fe3+>I2 |
| D | 向浓度均为0.1mol•L-1的KCl、KI混合溶液中滴加1~2滴0.01mol•L-1的AgNO3溶液,产生的沉淀呈黄色 | Ksp(AgCl)<Ksp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2、H2S | B. | SO2、NO2 | C. | CO2、NH3 | D. | SO2、Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
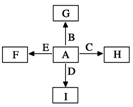 如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.
如图中,A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物. ,它的空间构型是直线型分子;
,它的空间构型是直线型分子;查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高一上10月月考化学试卷(解析版) 题型:选择题
在标准状况下,1体积水溶解672体积氨气,所得溶液密度为0.9g·cm-3,这种氨水的物质的量浓度和溶质的质量分数分别为( )
A.17.9mol·L-1 34.7% B.20.4mol·L-1 33.8%
C.17.9mol·L-1 33.8% D.20.4mol·L-1 34.7%
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
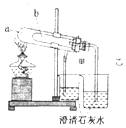 某研究性学习小组根据老师的学案设计实验对碳酸钠和碳酸氢钠的性质进行研究.
某研究性学习小组根据老师的学案设计实验对碳酸钠和碳酸氢钠的性质进行研究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com