
| A、1:1 | B、4:3 |
| C、2:3 | D、3:4 |
| 24 |
| 2 |
| m |
| X |
| 54 |
| 6 |
| m |
| Y |
| m |
| 12 |
| m |
| 9 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、离子半径的大小顺序为:r(W2-)>r(Q-)>r(Y2-)>r(Z3+) |
| B、元素W的最高价氧化物对应水化物的酸性比Q的强 |
| C、元素X的氢化物与Q的氢化物化合的产物中既含共价键又含离子键 |
| D、X、Y形成的化合物是大气污染物之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则a≤b-1 |
| B、在滴酚酞溶液的氨水中,加入NH4Cl至溶液恰好无色,则此时溶液的c (NH4+)=c(Cl-) |
| C、常温下,某硫酸溶液的pH=3,升高其温度,溶液pH增大 |
| D、相同温度、相同体积、相同物质的量浓度的KI和KF溶液中,离子总数前者大于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、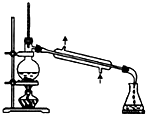 常用于分离互不相溶液体混合物 |
B、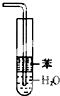 可用于吸收HCl气体,并能防倒吸 |
C、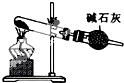 可用于实验室制NH3 |
D、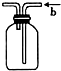 b口进气可收集CO2、NO等气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、④⑤ |
| C、①②③ | D、①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当25Cl=0.1V2时;c(A-)>c(B-) |
| B、当PH>7时,;c(A-)>c(OH-) |
| C、当pH=7,且V2=25 时,C1>0.1 |
| D、当PH<7 时,c(B+)>c(A-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com