
 ������Ҫ���л��ϳ��м��壬�㷺Ӧ�����ܼ������ܼ������ϡ���֯�ȹ�ҵ������������ʵ���Һ�ҵ�Ʒ����£�
������Ҫ���л��ϳ��м��壬�㷺Ӧ�����ܼ������ܼ������ϡ���֯�ȹ�ҵ������������ʵ���Һ�ҵ�Ʒ����£�| ͬһ��Ӧʱ�� | ͬһ��Ӧ�¶� | ||||
| ��Ӧ�¶� | ת���ʣ�%�� | ѡ���ԣ�%�� | ��Ӧʱ�� | ת���ʣ�%�� | ѡ���ԣ�%�� |
| 40�� | 77.8 | 100 | 2h | 80.2 | 100 |
| 60�� | 92.3 | 100 | 3h | 87.8 | 100 |
| 80�� | 92.6 | 100 | 4h | 92.3 | 100 |
| 120�� | 94.5 | 98.7 | 6h | 93 | 100 |
| ע��ѡ����100%��ʾ��Ӧ���ɵIJ���������������ˮ | |||||
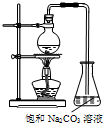
���� ��1����������ת���ʣ���ʹƽ�������ƶ�������Ӧ����С������Ũ�Ⱦ��ɣ�
��2��ͼʾװ���Ʊ�������������������ƫ�ͣ�ԭ�������ʵͻ��¶ȸ߷�������Ӧ��
��3����Ũ����Ϊ����ʱ���������Է�Һ����Ũ����ʹԭ��̿����
��4���ɱ������ݿ�֪��60�桢4hת���ʽϴ�ѡ���Ըߣ��ﵽ120��ʱ��ѡ���Խ������Ҵ���������Ӧ���������йأ�
��� �⣺��1������������ת���ʣ��ɲ�ȡ�Ĵ�ʩ�������Ҵ�Ũ�ȡ���ȥ������ȣ�
�ʴ�Ϊ�������Ҵ�Ũ�ȡ���ȥ�����
��2��������ͼ��ʾװ���Ʊ�������������������ƫ�ͣ���ԭ����ԭ����������Ӧ�ͱ����������¶ȹ��߷�������Ӧ��������Ч�����ã����ֲ���ӷ���
�ʴ�Ϊ��ԭ����������Ӧ�ͱ����������¶ȹ��߷�������Ӧ��
��3���˷�Ӧ��Ũ����Ϊ���������ܻ���ɲ����������Է�Һ��Ⱦ��������ԭ��̿����������ظ�ʹ�����ѣ�����Ч��������ȣ�
�ʴ�Ϊ�������������Է�Һ��Ⱦ��������ԭ��̿����
��4�����ɱ������ݿ�֪��60�桢4hת���ʽϴ�ѡ���Ըߣ��ʴ�Ϊ��C��
�ڴﵽ120��ʱ����Ӧѡ���Խ��͵�ԭ��������Ҵ���ˮ�������ѣ��ʴ�Ϊ���Ҵ���ˮ�������ѣ�
���� ���⿼���л�����Ʊ�ʵ�飬Ϊ��Ƶ���㣬���շ�Ӧԭ����ƽ���ƶ����л��������Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע����������ݵķ�����Ӧ�ã���Ŀ�ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C+O2 $\frac{\underline{\;��ȼ\;}}{\;}$CO2 ���Ϸ�Ӧ | |
| B�� | CaCO3$\frac{\underline{\;��ȼ\;}}{\;}$ CaO+CO2���ֽⷴӦ | |
| C�� | AgNO3+KCl�TAgCl��+KNO3���ֽⷴӦ | |
| D�� | Fe2O3+3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2 �û���Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ʵ�鲽�� | Ԥ������ͽ��� |
| ����1��ȡ��������Һ�����ˣ����ϴ�Ӻ�ȡ�������Թ��У��������2mol/L��������Һ��������ٵμӼ���0.1mol/L�Ȼ�����Һ | �а�ɫ��������˵������Һ�л���Cu4��OH��6SO4�� |
| ����2����ȡ��������Һ���Թ��У����Թܷ���װ�з�ˮ��С�ձ���ˮԡ����һ��ʱ��ȡ���Թܹ۲� | �Թ����к�ɫ�������ɣ�˵������Һ�л���Cu��OH��2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
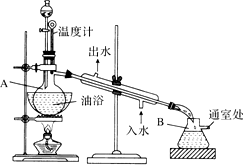 ������������ɫ����ˮ����ζ��Һ�壬�е�77.1�棬ʵ����ij����ȡ���ñ�����14.3mL��95%�Ҵ�23mL�����õ�ŨH2SO4������Na2CO3��Һ�Լ��������Ҵ���ϳ�����������Ȼ�����Һ����Ҫ����װ����ͼ��ʾ��ʵ�鲽���ǣ�������A������ƿ��ע�������Ҵ������õ�ŨH2SO4��ҡ�ȣ��ٽ�ʣ�µ������Ҵ��ͱ�����ע���Һ©�����ã���ʱ��Һ©�����Ҵ������������ʵ���֮��ԼΪ7��5���ڼ�����ԡ�������¶���135�桫145��֮�䣻�۽���Һ©���е�Һ�建������������ƿ����ڼ����ٶ�ʹ���������ٶ�������ٶȴ�����ȣ�ֱ��������ɣ��ܱ�����ԡ�¶�һ��ʱ�䣬��������Һ�������ֹͣ���ȣ���ȡ��B����ƿ����һ��������Na2CO3��Һ����������εؼӵ����Һ��ӱ�ҡ����ֱ�������ݲ���Ϊֹ�����ݵ�Һ�������Һ����ȥˮ�㣻�߽�����CaCl2��Һ�����������뵽��Һ©���У�ҡ��һ��ʱ�侲�ã��ų�ˮ�㣨��Һ�������Һ©����õ����dz����ᴿ������������Ʒ����Ȼ���������м�����ˮ�����ƣ���
������������ɫ����ˮ����ζ��Һ�壬�е�77.1�棬ʵ����ij����ȡ���ñ�����14.3mL��95%�Ҵ�23mL�����õ�ŨH2SO4������Na2CO3��Һ�Լ��������Ҵ���ϳ�����������Ȼ�����Һ����Ҫ����װ����ͼ��ʾ��ʵ�鲽���ǣ�������A������ƿ��ע�������Ҵ������õ�ŨH2SO4��ҡ�ȣ��ٽ�ʣ�µ������Ҵ��ͱ�����ע���Һ©�����ã���ʱ��Һ©�����Ҵ������������ʵ���֮��ԼΪ7��5���ڼ�����ԡ�������¶���135�桫145��֮�䣻�۽���Һ©���е�Һ�建������������ƿ����ڼ����ٶ�ʹ���������ٶ�������ٶȴ�����ȣ�ֱ��������ɣ��ܱ�����ԡ�¶�һ��ʱ�䣬��������Һ�������ֹͣ���ȣ���ȡ��B����ƿ����һ��������Na2CO3��Һ����������εؼӵ����Һ��ӱ�ҡ����ֱ�������ݲ���Ϊֹ�����ݵ�Һ�������Һ����ȥˮ�㣻�߽�����CaCl2��Һ�����������뵽��Һ©���У�ҡ��һ��ʱ�侲�ã��ų�ˮ�㣨��Һ�������Һ©����õ����dz����ᴿ������������Ʒ����Ȼ���������м�����ˮ�����ƣ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
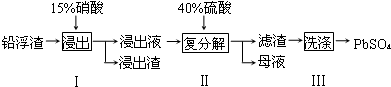
| ��ѧʽ | CaSO4 | Ag2SO4 | PbSO4 |
| Ksp | 4.9��10-5 | 1.2��10-5 | 1.6��10-8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
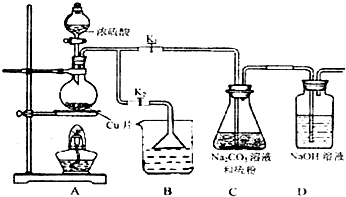
| ��� | 1 | 2 | 3 | 4 |
| ����Na2S2O3����Һ�����/mL | 18.02 | 17.98 | 18.00 | 20.03 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
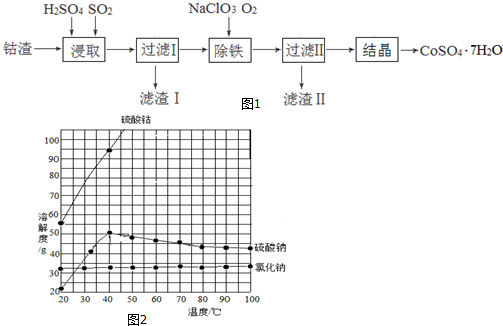
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com