
用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 2 mL 0.5 mol/L硅酸钠溶液中滴入盐酸所制得的硅酸胶体中,含胶粒数目为0.001 NA
B. 8.4 g NaHCO3固体中含有的离子总数为0.3 NA
C. 25℃时,1 L pH=l的CH3COOH溶液中含有氢离子数目为0.l NA
D. 7.8 g 过氧化钠固体中含有的共用电子对数目为0.2NA
科目:高中化学 来源:2017届山西省名校高三下学期联考理综化学试卷(解析版) 题型:简答题
亚氯酸钠是一种高效氧化性漂白剂。主要用于棉纺、亚麻、纸浆漂白、食品消毒、水处理、杀菌灭藻和鱼药制造。某化学兴趣小组对亚氯酸进行了研究,请回答下列问题。
已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出的晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaC1。
(1)下列物质中与亚氯酸钠漂白原理相同的是_______。
A.H2O2 B.NaClO C.SO2 D.Al(OH)3胶体
(2)现利用下图所示装置(夹持装置省略)进行制取NaClO2晶体实验。
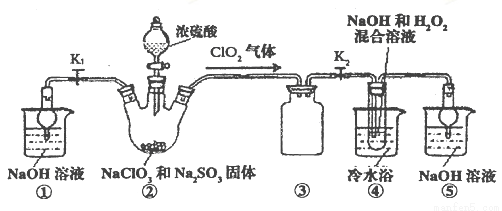
a.装置②中两种实验仪器的名称分别是_____________ 、___________。
b.装置②中产生ClO2的化学方程式为_________________________。
装置④中制备NaClO2的离子方程式为________________________。
c.装置③的作用是________________。
d.未反应完的ClO2在装置⑤中可被NaOH溶液吸收,生成的氧化产物与还原产物均为含氧酸盐,且二者的物质的量之比为1:1,请写出该反应的离子方程式______________________。
e.从装置④反应后的溶液获得NaClO2晶体的操作步骤如下:
①减压,55℃蒸发结晶;②趁热过滤;③___________;④低于60℃干燥,得到成品。
(3)用如下实验方案测定亚氯酸钠样品的纯度。
亚氯酸钠样品纯度测定实验用到的化学反应方程式为ClO2-+4I-+4H+=2H2O+2I2+Cl-、I2+2S2O32-=2I-+S4O62-
a.该测定实验用到的指示剂为_________________。
b.为测定亚氯酸钠样品纯度,需要用到下列实验数据中的___________(填写选项字母)
A.亚氯酸钠样品的质量(a g)
B.过量的碘化钾晶体的质量(b g)
C.稀硫酸的浓度(cmol/L)和体积(D mL)
D.指示剂的加入量(d mol)
E.标准液的浓度(e mol/L)和消耗体积(VmL)
用上述选定的数据表示出样品中NaC1O2 质量分数____________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期基础训练(15)化学试卷(解析版) 题型:实验题
如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:

(1)该浓盐酸中HCl的物质的量浓度为__________mol·L-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是_____。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液的密度 D.溶液中Cl-的数目
(3)下列容量瓶的使用方法中,不正确的是____________
A.使用容量瓶前检验是否漏水
B.容量瓶用水洗净后,再用待配溶液洗涤
C.配制溶液时,如果试样是固体,把称好的固体用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
D.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流倒入容量瓶中,缓慢加水至刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线。
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
(4)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.200 mol·L-1的稀盐酸。
①该学生需要用量筒量取________mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作会使所配制的稀盐酸的物质的量浓度偏大的有_____
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容。
B.用量筒量取浓盐酸时俯视观察凹液面。
C.在容量瓶中定容时俯视刻度线。
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线,又加水至刻度线。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期基础训练(15)化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数,下列叙述正确的是
A. 28gC2H4所含共用电子对数目为4NA
B. 1L0.1mol·L-1乙酸溶液中H+数为0.1NA
C. 1mol甲烷分子所含质子数为10NA
D. 标准状况下,22.4L乙醇的分子数为NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期基础训练(15)化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的值,下列叙述正确的是
A. 60g丙醇中存在的共价键总数为10NA
B. 1L 0.1 mol·L-1的NaHCO3溶液中HCO3-和CO32-的离子数之和为0.1NA
C. 钠在空气中燃烧可生成多种氧化物,23g钠充分燃烧时转移电子数为1 NA
D. 235g核素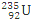 发生裂变反应:
发生裂变反应: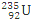 +
+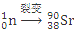 +
+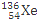 +10
+10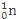 ,净产生的中子(
,净产生的中子(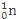 )数为10 NA
)数为10 NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期基础训练(15)化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的数值,下列说法正确的是
A. 1molCl2参加的任何反应,反应过程中转移电子数都是2NA
B. 标准状况下,11.2L乙醇所含的羟基数为0.5NA
C. 常温常压下,17g甲基(—14CH3)所含的中子数为9NA
D. 室温下,42.0 g乙烯和丙烯的混合气体中含有的碳原子数约为3×6.02×1023个
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省西安市高一上学期期末考试化学试卷(解析版) 题型:选择题
用下列方法配制相应的溶液,所配制的溶液浓度偏高的是 ( )
①用1 g 98%的浓硫酸加4 g水配制成19.6%的硫酸;
②配制一定物质的量浓度的硫酸溶液时,定容后,塞好塞子倒转摇匀后,发现液面低于刻度线;
③10%的硫酸和90%的硫酸等体积混合配制50%的硫酸溶液;
④向80 mL水中加入18.4 mol/L硫酸20 mL,配制3.68mol/L的硫酸溶液;
⑤质量分数为5x%和x%的两种氨水等体积混合配制成3x%的氨水
A. ①③⑤ B. ②③ C. ③④ D. ④⑤
查看答案和解析>>
科目:高中化学 来源:浙江省衢州市2017届高三1月教学质量检测化学试卷 题型:计算题
X常温下是一种无色液体,极易水解,遇潮湿空气会产生白雾。实验室制备X可用A、C两种气体发生化合反应制得,物质转化过程如下:
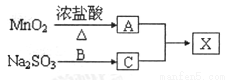
为探究X的组成,取13.5gX与足量水完全反应,在生成物中加入1.0mol/L的NaOH溶液40.0mL恰好显中性。继续加入过量BaCl2溶液,产生沉淀2.33g。
请回答:
(1)由Na2SO3和B反应生成C的离子方程式______________
(2)X的分子式是________。在生成X的反应中,C表现了___________性。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com