
【题目】20℃时,饱和NaCl溶液的密度为ρ g·cm-3,物质的量浓度为c mol·L-1,则下列说法中错误的是( )
A.温度低于20℃时,饱和NaCl溶液的浓度小于c mol·L-1
B.20℃时,饱和NaCl溶液的质量分数为![]() ×100%
×100%
C.20℃时,密度小于ρ g·cm-3的NaCl溶液是不饱和溶液
D.20℃时,饱和NaCl溶液的溶解度S=![]()
科目:高中化学 来源: 题型:
【题目】(1)在一定条件下,28.80g金属单质A与1.20molCl2完成反应,生成1.20molAClx,则x=__________,若A原子核内质子数等于中子数,则A原子核内中子数为__________ ,氯原子结构示意图为____________。
(2)现有氨气3.4g,在标准状况下其体积为____________,含有氮原子的数目为_____ ;将气体全部溶于水,配成500mL溶液,该溶液的物质的量浓度为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
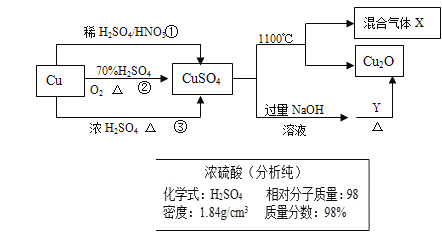
【题目】CuSO4是一种重要化工原料,其制备和有关性质如图所示。
(1)现要用如图所示的浓硫酸来配制步骤①中所需要的1mol/L的稀硫酸480ml,需要用这种浓硫酸的体积为______ml。
(2)配制该稀硫酸所用到的玻璃仪器除玻璃棒、量筒、烧杯外还有_______、__________。
(3)下列操作会使所配溶液浓度偏低的是 _________。
A. 硫酸转移至容量瓶后,没有洗涤烧杯
B. 未冷却至室温就转移至容量瓶
C. 容量瓶中存在少量蒸馏水
D. 定容时俯视刻度 E.量取浓硫酸时量筒内有少量蒸馏水
(4)制取硫酸铜的途径①②③中,途径_________能更好地体现绿色化学的思想。
(5)配制1000ml 0.1mol/L的硫酸铜溶液,需用托盘天平称取________g胆矾。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组欲探究一盒遗失了说明书的治疗胃酸过多的抗酸药片的有效成分。首先,查阅资料得知:抗酸药通常由数种物质组成,其中有效成分为碳酸氢钠、氢氧化镁、氢氧化铝、碳酸钙中的一种或几种。然后进行了如下实验:
Ⅰ.将两片抗酸药片研磨后,装入一支试管中。
Ⅱ.向该试管中加入过量盐酸,产生无色气体.过滤后得到无色溶液。
Ⅲ.用铂丝蘸取少量Ⅱ中所得溶液,在酒精灯外焰上灼烧,无黄色火焰。
Ⅳ.向Ⅱ中所得溶液中滴加NaOH溶液,产生白色沉淀。
请回答:
(1)Ⅱ中产生无色气体的离子方程式是____________。
(2)甲同学由实验Ⅳ判断该抗酸药片中一定含有氢氧化铝,乙同学认为不合理。乙同学判断的依据是________。于是,乙同学设计实验V进行探究:取实验Ⅳ中的白色沉淀于另一支试管中,滴加足量的NaOH溶液,沉淀部分溶解,相应的离子方程式是__________。
(3)通过上述实验,得出的结论是:该抗酸药片的有效成分为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以乙醇为原料,用下述6种类型的反应:①氧化,②消去,③加成,④酯化,⑤水解,⑥加聚,来合成乙二酸乙二酯(![]() )的正确顺序是( )
)的正确顺序是( )
A. ①⑤②③④B. ①②③④⑤
C. ②③⑤①⑥D. ②③⑤①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F六种有机物,它们的转化关系如图所示(图中部分反应条件及生成物没有全部写出).已知:液体B能发生银镜反应,气体D的相对分子质量为28.
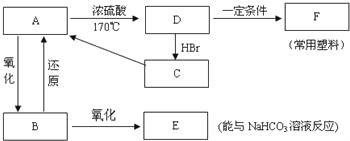
(1)A、B、C的结构简式分是 、 、 .
(2)B、C中所含官能团的名称分别是 、 .
(3)A到D的反应类型为 .
(4)C→A的反应条件是 .
(5)D→F反应的化学方程式是 .
(6)在一定的条件下,A与E反应可生成一种具有香味的物质.该反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关气体体积的叙述正确的是( )
A.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子大小决定
B.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子数决定
C.不同的气体,若体积不同,则它们所含的分子数也不同
D.气体摩尔体积指1mol任何气体所占的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高纯度单晶硅是典型的无机非金属材料,又称“半导体”材料,它的发现和使用曾引起计算机的一场“革命”。这种材料可以按下列方法制备:
SiO2![]() Si(粗)
Si(粗)![]() SiHCl3
SiHCl3![]() Si(纯),下列说法正确的是( )
Si(纯),下列说法正确的是( )
A.步骤①的化学方程式为SiO2+C![]() Si+CO2↑
Si+CO2↑
B.步骤①、②、③中每生成或反应1 mol Si,转移4 mol电子
C.二氧化硅能与氢氟酸反应,而硅不能与氢氟酸反应
D.SiHCl3(沸点33.0 ℃)中含有少量的SiCl4(沸点67.6 ℃),通过蒸馏(或分馏)可提纯SiHCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水杨酸冬青油、阿司匹林的结构简式如图,下列说法不正确的是

A. 由水杨酸制冬青油的反应是取代反应
B. 阿司匹林的分子式为C9H8O4,在一定条件下水解可得水杨酸
C. 冬青油苯环上的一氯取代物有4种
D. 可用NaOH溶液除去冬青油中少量的水杨酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com