
【题目】现有短周期主族元素X、Y、Z、R、T。R原子最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Z与T形成的Z2T 化合物能破坏水的电离平衡,五种元素的原子半径与原子序数的关系如图所示,下列推断正确的是

A. 原子半径和离子半径均满足:Y<Z
B. Y的单质易与R、T的氢化物反应
C. 最高价氧化物对应的水化物的酸性:T<R
D. 由X、R、Y、Z四种元素组成的化合物水溶液一定显碱性
【答案】B
【解析】
现有短周期主族元素X、Y、Z、R、T,结合五种元素的原子半径与原子序数的关系图可知,Z的原子半径最大,X的原子半径和原子序数均最小,则X为H元素;由R原子最外层电子数是电子层数的2倍,R为第二周期的C元素;Y与Z能形成Z2Y、Z2Y2型离子化合物,则Z为Na元素,Y为O元素,Z与T形成的Z2T化合物能破坏水的电离平衡,T为S元素,据此分析解答。
由上述分析可知,X为H元素,R为C元素,Y为O元素,Z为Na元素,T为S元素。
A.电子层越多,原子半径越大,则原子半径为Y<Z,而具有相同电子排布的离子中原子序数大的离子半径小,则离子半径为Y>Z,故A错误;
B.Y的单质为氧气,与C的氢化物能够发生燃烧反应,与S的氢化物能够反应生成S和水,故B正确;
C.非金属性S>C,则最高价氧化物对应的水化物的酸性:T>R,故C错误;
D.由H、C、O、Na四种元素组成的化合物不仅仅为NaHCO3,可能为有机盐且含有羧基,溶液不一定为碱性,可能为酸性,如草酸氢钠溶液显酸性,故D错误;
答案选B。


 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:
【题目】I.下面是甲、乙、丙三位同学制取乙酸乙酯的过程,请你参与完成相关实验问题讨论。
(实验目的)制取乙酸乙酯
(实验原理)甲、乙、丙三位同学均采取乙醇、乙酸与浓硫酸混合共热的方法制取乙酸乙酯。
(装置设计)甲、乙、丙三位同学分别设计了下列三套实验装置:

根据分析回答:(1)三位同学设计的装置中最不合理的是____(选填“甲”或“乙”或“丙”),原因是_________________。
(实验步骤)
a.按所选择的装置组装仪器,在试管①中先加入3mL乙醇,并在摇动下缓缓加入2mL浓硫酸充分摇匀,冷却后再加入2mL冰醋酸;
b.将试管固定在铁架台上;
c.在试管②中加入适量的饱和Na2CO3溶液;
d.用酒精灯对试管①加热;
e.当观察到试管②中有明显现象时停止实验。
(2)试管①中加入浓硫酸的作用是______________________________
(3)该实验中长导管的作用是___________________。
(4)试管②中饱和Na2CO3溶液的作用是_______________;可否用NaOH溶液代替Na2CO3溶液?_____(填“是”或“否”),理由是用化学方程式回答_______________。
(5)写出试管①中乙醇工业制取的化学方程式________________________________;
II.实验室制备硝基苯的主要步骤如下:
a、配制一定比例的浓H2SO4与浓HNO3的混合酸,加入反应器中;
b、向室温下的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
c、在55~60℃下发生反应,直至反应结束;
d、除去混合酸后,粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤;
e、将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯净硝基苯。请填写下列空白:
①制备硝基苯的反应类型是________________。
②配制一定比例的浓H2SO4与浓HNO3的混合酸时,操作的注意事项是:_____。
③步骤d中洗涤、分离粗硝基苯应使用的仪器是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用废铁屑制备磁性胶体粒子,制取过程如下:

下列说法不正确的是
A. 用Na2CO3溶液浸泡是为了除去废铁屑表面的油污
B. 通入N2是防止空气中的O2氧化二价铁元素
C. 加适量的H2O2是为了将部分Fe2+氧化为Fe3+,涉及反应:H2O2+2Fe2++2H+=2Fe3++2 H2O
D. 溶液A中Fe2+和Fe3+的浓度比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2A在水中存在以下平衡:H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2-。回答以下问题:
H++A2-。回答以下问题:
(1)NaHA溶液_______(填“显酸性”“显碱性”“显中性”或“酸碱性无法确定”),原因是_________________________________________________________。
(2)某温度下,向0.1 mol·L-1的NaHA溶液中滴入0.1 mol·L-1KOH溶液至中性,此时溶液中以下关系一定正确的是__________(填字母)。
A.c(H+)·c(OH-)=1×10-14
B.c(Na+)+c(K+)=c(HA-)+2c(A2-)
C.c(Na+)>c(K+)
D.c(Na+)+c(K+)=0.05 mol·L-1
(3)已知常温下H2A的钙盐(CaA)饱和溶液中存在以下平衡:CaA(s) ![]() Ca2+(aq)+A2-(aq) ΔH>0。
Ca2+(aq)+A2-(aq) ΔH>0。
①温度升高时,Ksp_________(填“增大”“减小”或“不变”,下同)。
②滴加少量浓盐酸,c(Ca2+)_________,原因是_____________________ (用文字和离子方程式说明)。
(4)若向CaA悬浊液中加入CuSO4溶液,生成一种黑色固体物质,写出该过程中反应的离子方程式:__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重2.2 g。回答下列问题:
(1)2.3 g A中所含氢原子、碳原子的物质的量各是多少_____?
(2)通过计算确定该有机物的分子式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g)![]() Fe(s)+CO2(g)(正反应是吸热反应),其平衡常数可表示为K=
Fe(s)+CO2(g)(正反应是吸热反应),其平衡常数可表示为K=![]() ,已知1100℃时K=0.263
,已知1100℃时K=0.263
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值________;平衡常数K值___________ (选填“增大”“减小”或“不变”)。
(2)1100℃时测得高炉中c(CO2)=0.025mol·L﹣1、c(CO)=0.1mol·L﹣1,在这种情况下,该反应是否处于化学平衡状态_________ (选填“是”或“否”),此时,化学反应速率是υ(正)_______ υ(逆)(选填“大于”“小于”或“等于”),其原因是____________。
(3)能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ.CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH=+206.0 kJ/mol
Ⅱ.CO(g)+2H2(g)=CH3OH(g)ΔH=-129.0 kJ/mol
CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
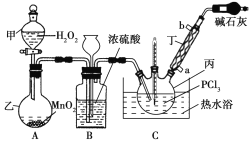
【题目】三氯氧磷(POCl3)是一种工业化工原料,可用于制取有机磷农药、长效磺胺药物等,还可用作染料中间体、有机合成的氯化剂和催化剂、阻燃剂等。利用O2和PCl3为原料可制备三氯氧磷,其制备装置如图所示(夹持装置略去):
已知PCl3和三氯氧磷的性质如表:
熔点/℃ | 沸点/℃ | 其他物理或化学性质 | |
PCl3 | -112.0 | 76.0 | PCl3和POCl3互溶,均为无色液体,遇水均剧烈水解,发生复分解反应生成磷的含氧酸和HCl |
POCl3 | 1.25 | 106.0 |
(1)装置A中的分液漏斗能否用长颈漏斗代替?做出判断并分析原因:_______
(2)装置B的作用是______________(填标号)。
a.气体除杂 b.加注浓硫酸 c.观察气体流出速度 d.调节气压
(3)仪器丙的名称是___________,实验过程中仪器丁的进水口为__________(填“a”或“b”)口。
(4)写出装置C中发生反应的化学方程式_______,该装置中用温度计控制温度为60~65 ℃,原因是________。
(5)称取16.73 g POCl3样品,配制成100 mL溶液;取10.00 mL溶液于锥形瓶中,加入3.2 mol·L-1的AgNO3溶液10.00 mL,并往锥形瓶中滴入5滴Fe2(SO4)3溶液;用0.20 mol·L-1的KSCN溶液滴定,达到滴定终点时消耗KSCN溶液10.00 mL(已知:Ag++SCN-=AgSCN↓)。则加入Fe2(SO4)3溶液的作用是________,样品中POCl3的纯度为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式书写正确的是
A.硝酸铝溶液中滴加过量氨水:Al3++4NH3·H2O=AlO2-+4NH4+↑+2H2O
B.用铝粉和NaOH溶液反应制取大量H2:Al+2OH-=AlO2-+H2↑
C.实验室制取Cl2:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
D.氯气溶于水,与水的反应:Cl2+H2O=2H++Cl-+ClO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氢元素可形成种类繁多的烃类物质。
(1)下图表示某些烃分子的模型:
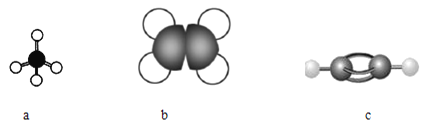
①写出a分子的空间构型______。
②c分子中的一个氢原子被![]() —取代后的物质共直线的原子最多有______个。
—取代后的物质共直线的原子最多有______个。
③取等质量的上述三种烃充分燃烧,耗氧量最大的是______(填分子式)。
④25℃和101kPa时,取a、b和c组成的混合烃32mL,与过量氧气混合并完全燃烧,除去水蒸气,恢复到原来的温度和压强,气体总体积缩小了56mL,原混合烃中c的体积分数为______。
(2)某烯烃的结构简式如下所示:
![]()
①用系统命名法对该烃与![]() 的加成产物命名:______,该加成产物的—氯取代物有______种。
的加成产物命名:______,该加成产物的—氯取代物有______种。
②该烯烃可以加聚生成高分子,写出该高聚物的结构简式______。该烯烃还能与乙烯以1:1比例反应形成一种环状化合物,请写出该环状化合物的键线式______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com