
铁矿石是工业炼铁的主要原料之一,其主要成分为铁的氧化物(假设杂质中不含铁元素和氧元素,且杂质不与稀硫酸反应)。某研究性学习小组对某铁矿石中铁的价态和氧化物的化学式进行探究。
[提出假设]
假设1:铁矿石中只含+3价铁;
假设2:铁矿石中只含+2价铁;
假设3:_____________________________________________。
[查阅资料]2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
[定性探究]
实验(一)
取铁矿石样品粉碎,盛装于烧杯中,加入适量的X溶液,微热,充分溶解后将滤液分成四份:
①向第一份溶液中滴加少量KSCN溶液;
②向第二份溶液中滴加适量高锰酸钾溶液;
③向第三份溶液中滴加少量KSCN溶液,再滴加适量过氧化氢溶液;
④向第四份溶液中滴加适量氢氧化钠溶液。
(1)上述X溶液是________(填“稀硝酸”“稀硫酸”或“浓盐酸”);上述方案中,一定能证明铁矿石中含+2价铁的方案是________(填序号)。
[定量探究]
实验(二) 铁矿石中含氧量的测定:
①按图组装仪器,检查装置的气密性;
②将5.0 g铁矿石放入硬质玻璃管中,其他装置中的药品如图所示(夹持装置已略去);
③A中开始反应,不断地缓缓向后续装置中通入氢气,待D装置出口处氢气验纯后,点燃C处酒精灯;
④充分反应后,撤掉酒精灯,再持续通入氢气直至完全冷却。
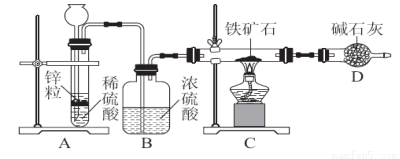
(2)按上述方案进行多次实验,假设各项操作都正确,但最终测得结果都偏高,请你提出改进方案的建议:____________________________________________________。
如果拆去B装置,测得结果可能会________(填“偏高”“偏低”或“无影响”)。
(3)改进方案后,测得反应后D装置增重1.35 g,则铁矿石中氧的百分含量为________。若将H2换成CO,则还需补充________装置。
实验(三) 铁矿石中含铁量的测定:
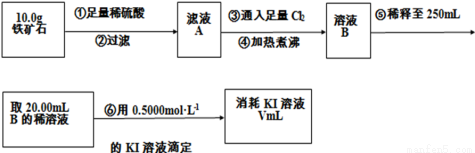
(4)步骤⑤中用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、______________。
(5)步骤④中煮沸的作用是_________________________________________。
(6)若滴定过程中消耗0.500 0 mol·L-1的KI溶液20.00 mL,则铁矿石中铁的百分含量为________。
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年河北省高二下期中化学试卷(解析版) 题型:选择题
短周期主族元素A、B形成AB3型分子,下列有关叙述正确的是( )
A.若A、B为同一周期元素,则AB3分子一定为平面正三角形
B.若AB3分子中的价电子个数为24个,则AB3分子为平面正三角形
C.若为A、B为同一主族元素,则 AB3分子一定为三角锥形
D.若AB3分子为三角锥形,则 AB3分子一定为 NH 3
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三高考模拟九化学试卷(解析版) 题型:选择题
化学与人类的生活密切相关,下列说法中正确的是
A.烧鱼时,先加酒后又加醋,产生香味是因为生成大量的乙酯乙酯
B.在鸡蛋清中加入食盐,搅拌均匀,静置后会出现凝聚现象
C.纯碱水溶液呈碱性,纯碱属于碱类
D.SO2有漂白作用,可用于食材的漂白
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三高考模拟八化学试卷(解析版) 题型:选择题
下表各组物质中,物质之间不可能实现如图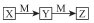 所示转化
所示转化
选项 | X | Y | Z | M |
A | Fe(s) | FeCl2 | FeCl3 | Cl2 |
B | NaOH(aq) | Na2CO3 | NaHCO3 | CO2 |
C | NH3(g) | NO | NO2 | O2 |
D | S(s) | SO2 | SO3 | O2 |
查看答案和解析>>
科目:高中化学 来源:2016届海南中学高三高考模拟八化学试卷(解析版) 题型:选择题
化学与生活、生产密切相关,下列说法错误的是
A.大力防治 PM2.5 的污染防治,可减少雾霾天气
B.“84 消毒液”具有强氧化性,可作环境的消毒剂
C.发展低碳经济,利用太阳能、风能实现城市照明
D.可以用福尔马林溶液保存海鲜产品
查看答案和解析>>
科目:高中化学 来源:2016届青海省西宁市等校高三下联考理综化学试卷(解析版) 题型:选择题
用下列实验装置进行相应实验,能达到实验目的的是( )
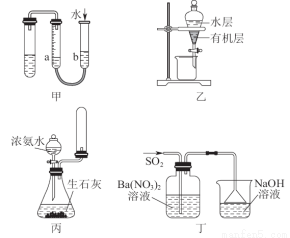
A.用图甲的方法不能检查此装置的气密性
B.图乙可以作为CCl4萃取溴水后的分液装置
C.实验室用图丙所示装置制取少量氨气
D.图丁洗气瓶中的白色沉淀为BaSO3
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三5月月考理综化学试卷(解析版) 题型:填空题
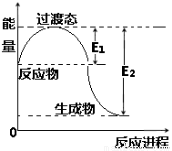
Ⅰ.(1)右图为1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图。已知E1=134KJ/mol,E2=368KJ/mol( E1、 E2为反应的活化能)。若在反应体系中加入催化剂,反应速率增大,则E1、△H的变化分别是 、 (填“增大”、“减小”或“不变”)。写出该 反应的热化学方程式 。
(2)若反应SO2(g)+I2(g)+2H2O(g)=H2SO4(l)+2HI(g)在150℃下能自发进行,则△H___0。
A.大于 B.小于 C.等于 D.大于或小于都可
Ⅱ.以CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应:
2CO2(g)+6H2(g)  CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
CH3CH2OH(g)+3H2O(g) △H=QkJ/mol (Q>0)
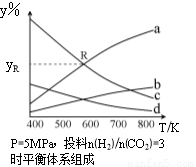
在密闭容器中,按CO2与H2的物质的量之比为1:3进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如下图所示。完成下列填空:
(1)表示CH3CH2OH体积分数曲线的是____(选填序号)。
(2)在一定温度下反应达到平衡的标志是 。
A.平衡常数K不再增大 B.CO2的转化率不再增大
C.混合气体的平均相对分子质量不再改变 D.反应物不再转化为生成物
(3)其他条件恒定,达到平衡后,能提高H2转化率的措施是_______(选填编号)。
A.升高温度 B.充入更多的H2 C.移去乙醇 D.增大容器体积
(4)图中曲线a和c的交点R对应物质的体积分数yR=_______。
查看答案和解析>>
科目:高中化学 来源:2016届湖北省沙市高三下高考第一次模拟理综化学试卷(解析版) 题型:选择题
有机物X只含C、H、O三种元素,其相对分子质量不超过100,若X中所含氧元素的质量分数为36.36%,则能与NaOH溶液发生反应的X共有(不考虑立体异构)
A.5种 B.6种 C.7种 D.8种
查看答案和解析>>
科目:高中化学 来源:2015-2016学年黑龙江牡丹江一中高一下期中化学试卷(解析版) 题型:选择题
下列不能使溴水完全褪色的是( )
A.碳酸钠 B.氢氧化钾溶液 C.二氧化硫 D.KI溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com