
ČéĖį·Ö×ÓŹ½ĪŖC3H6O3£¬ŌŚŅ»¶ØµÄĢõ¼žĻĀæÉ·¢ÉśŠķ¶ą»Æѧ·“Ó¦£¬ĻĀĶ¼ŹĒ²ÉÓĆ»Æѧ·½·Ø¶ŌČéĖį½ųŠŠ¼Ó¹¤“¦ĄķµÄ¹ż³Ģ£¬ĘäÖŠA”¢H”¢GĪŖĮ“דøß·Ö×Ó»ÆŗĻĪļ£®£ØŅŃÖŖ﹣OH£¬﹣COOHµČĪŖĒ×Ė®»łĶÅ£¬F³£×öÄŚČ¼»śµÄ湶³¼Į£©Ēė»Ų“šĻą¹ŲĪŹĢā£ŗ
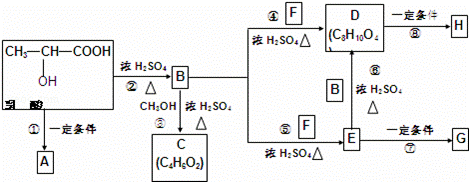
£Ø1£©ĶʶĻ½į¹¹¼ņŹ½£¬C£ŗ””””£»F£ŗ””””£®
£Ø2£©BÖŠĖłŗ¬µÄ¹ŁÄÜĶÅÓŠ””””£»·“Ó¦¢ŪµÄ·“Ó¦ĄąŠĶŹĒ””””£®
£Ø3£©·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½ĪŖ””””£®
£Ø4£©×÷ĪŖŅžŠĪŃŪ¾µµÄÖĘ×÷²ÄĮĻ£¬¶ŌĘäŠŌÄܵÄŅŖĒó³żÓ¦¾ßÓŠĮ¼ŗĆµÄ¹āѧŠŌÄÜĶā£¬»¹Ó¦¾ßÓŠĮ¼ŗƵÄĶøĘųŠŌŗĶĒ×Ė®ŠŌ£®Ņ»°ć²ÉÓĆEµÄ¾ŪŗĻĪļG¶ų²»ŹĒDµÄ¾ŪŗĻĪļHĄ“ÖĘ×÷ŅžŠĪŃŪ¾µ£¬ĘäÖ÷ŅŖĄķÓÉŹĒ””””£®
| ÓŠ»śĪļµÄĶʶĻ£® | |
| ×ØĢā£ŗ | ÓŠ»śĪļµÄ»ÆѧŠŌÖŹ¼°ĶʶĻ£® |
| ·ÖĪö£ŗ | ČéĖįÖŠŗ¬ÓŠ﹣OHŗĶ﹣COOH£¬Ņ»¶ØĢõ¼žĻĀÉś³ÉĮ“דøß·Ö×Ó»ÆŗĻĪļA£¬ŌņAĪŖ |
| ½ā“š£ŗ | ½ā£ŗČéĖįÖŠŗ¬ÓŠ﹣OHŗĶ﹣COOH£¬Ņ»¶ØĢõ¼žĻĀÉś³ÉĮ“דøß·Ö×Ó»ÆŗĻĪļA£¬ŌņAĪŖ £Ø1£©ÓÉŅŌÉĻ·ÖĪöæÉÖŖCĪŖCH2═CHCOOCH3£¬FĪŖHO﹣CH2CH2﹣OH£¬ ¹Ź“š°øĪŖ£ŗCH2═CHCOOCH3£»HO﹣CH2CH2﹣OH£» £Ø2£©BĪŖCH2═CHCOOH£¬ŗ¬ÓŠĢ¼Ģ¼Ė«¼ü”¢ōČ»ł¹ŁÄÜĶÅ£» ·“Ó¦¢ŪĪŖCH2═CHCOOHÓė¼×“¼·¢Éśõ„»Æ·“Ӧɜ³ÉCH2═CHCOOCH3£¬ ¹Ź“š°øĪŖ£ŗĢ¼Ģ¼Ė«¼ü”¢ōČ»ł£»õ„»Æ·“Ó¦»ņČ”“ś·“Ó¦£¬ £Ø3£©·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗ ¹Ź“š°øĪŖ£ŗ £Ø4£©¶Ō±ČD”¢EµÄ½į¹¹£¬Č·¶ØĖüĆĒµÄ¾ŪŗĻĪļH”¢G½į¹¹ÉĻµÄ²»Ķ¬µćŹĒGµÄ½į¹¹ÖŠ»¹ŗ¬ÓŠ“óĮæµÄ﹣OH£¬Ź¹øĆĪļÖŹ¾ßÓŠĒ×Ė®ŠŌ£¬¶ųHŌņ²»¾ßÓŠ£¬ĖłŅŌ¾ŪŗĻĪļGæÉŅŌÖĘ×÷ŅžŠĪŃŪ¾µ£¬ ¹Ź“š°øĪŖ£ŗøß¾ŪĪļGÖŠŗ¬ÓŠµÄ﹣OH£¬Ź¹øĆĪļÖŹ¾ßÓŠĒ×Ė®ŠŌ£¬¶ųHŌņ²»¾ßÓŠ£® |
| µćĘĄ£ŗ | ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻ£¬ĢāÄæÄŃ¶Č½Ļ“󣬽ā“š±¾ĢāµÄĶ»ĘĘæŚĪŖČéĖįµÄŠŌÖŹ£¬×¢Ņāøł¾ŻĖłŗ¬ÓŠµÄ¹ŁÄÜĶŽįŗĻ·“Ó¦µÄĢŲµćæÉÕżĶĘø÷ÓŠ»śĪļ£® |
””


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ»Æѧ·“Ó¦ŌŚ½šŹōŅ±Į¶¹¤ŅµÖŠ»¹Ć»ÓŠµĆµ½Ó¦ÓƵďĒ
””(””””)
A.2NaCl(ČŪČŚ) 2Na+Cl2”ü
2Na+Cl2ӟ
B.Al2O3+3C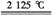 2Al+3COӟ
2Al+3COӟ
C.Fe2O3+3CO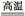 2Fe+3CO2
2Fe+3CO2
D.2Ag2O 4Ag+O2ӟ
4Ag+O2ӟ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ļņŗ¬ÓŠĻĀĮŠĄė×ÓµÄČÜŅŗÖŠ·Ö±š¼ÓČėÉÕ¼ī¹ĢĢå£ØČÜŅŗĢå»ż±ä»ÆæÉŗöĀŌ£©£¬ÄÜŅżĘšĄė×ÓÅØ¶Č¼õŠ”µÄŹĒ£Ø””””£©
| ”” | A£® | CO32﹣ | B£® | Cl﹣ | C£® | OH﹣ | D£® | Cu2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĀĢÉ«»ÆѧµÄŗĖŠÄŹĒ·“Ó¦¹ż³ĢµÄĀĢÉ«»Æ£¬ŅŖĒóŌĮĻĪļÖŹÖŠµÄĖłÓŠŌ×ÓĶźČ«±»ĄūÓĆĒŅČ«²æ×ŖČėĘŚĶūµÄ²śĘ·ÖŠ£®ĻĀĮŠ¹ż³Ģ²»·ūŗĻÕāŅ»Ė¼ĻėµÄŹĒ£Ø””””£©
| ”” | A£® | ¼×Ķ锢COŗĻ³ÉŅŅĖįŅŅõ„£ŗ2CH4+2CO |
| ”” | B£® | Ļ©ĢžÓėĖ®ĆŗĘų·¢ÉśµÄōŹ»łŗĻ³É·“Ó¦£ŗRCH=CH2+CO+H2 |
| ”” | C£® | ŅŅ“¼±»ŃõĘų“ß»ÆŃõ»Æ³ÉŅŅČ© |
| ”” | D£® | ĀČŅŅĻ©ŗĻ³É¾ŪĀČŅŅĻ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĪļÖŹ½ųŠŠŅ»ĀČČ”“ś·“Ó¦ŗó£¬Ö»ÄÜÉś³ÉĖÄÖÖ·Šµć²»Ķ¬²śĪļµÄĢžŹĒ£Ø””””£©
| ”” | A£® | £ØCH3£©2CHCH2CH2CH3 | B£® | £ØCH3CH2£©2CHCH3 |
| ”” | C£® | £ØCH3£©2CHCH£ØCH3£©2 | D£® | £ØCH3£©3CCH2CH3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¹ŲÓŚČČ»Æѧ·“Ó¦µÄĆčŹöÖŠÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | HClŗĶNaOH·“Ó¦µÄÖŠŗĶČČ”÷H=﹣57.3kJ/mol£¬ŌņH2SO4ŗĶCa£ØOH£©2·“Ó¦µÄÖŠŗĶČČ”÷H=2”Į£Ø﹣57.3£©kJ/mol |
| ”” | B£® | CO£Øg£©µÄČ¼ÉÕČČŹĒ283.0kJ/mol£¬Ōņ2CO2£Øg£©═2CO£Øg£©+O2£Øg£©·“Ó¦µÄ”÷H=+566.0kJ/mol |
| ”” | C£® | ŠčŅŖ¼ÓČČ²ÅÄÜ·¢ÉśµÄ·“Ó¦Ņ»¶ØŹĒĪüČČ·“Ó¦ |
| ”” | D£® | 1mol¼×ĶéČ¼ÉÕÉś³ÉĘųĢ¬Ė®ŗĶ¶žŃõ»ÆĢ¼Ėł·Å³öµÄČČĮæŹĒ¼×ĶéµÄČ¼ÉÕČČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
×ćĮæĆ¾·ŪÓėŅ»¶ØĮæµÄŃĪĖį·“Ó¦£¬ÓÉÓŚ·“Ó¦ĖŁĀŹĢ«æģ£¬ĪŖ¼õĀż·“Ó¦ĖŁĀŹ£¬µ«²¢²»Ó°ĻģĒāĘų²śÉśµÄ×ÜĮ棬æÉŅŌ¼ÓČėĻĀĮŠĪļÖŹÖŠµÄ£Ø””””£©
| ”” | A£® | MgO | B£® | NaOH | C£® | K2CO3 | D£® | CH3COONa |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½Ģ²ÄÖŠÓĆĖįŠŌKMnO4ŗĶH2C2O4£Ø²ŻĖį£©·“Ӧъ¾æÓ°Ļģ·“Ó¦ĖŁĀŹµÄŅņĖŲ£¬Ąė×Ó·½³ĢŹ½ĪŖ£ŗ2MnO4﹣+5H2C2O4+6H+═2Mn2++10CO2”ü+8H2O£®Ņ»ŹµŃ銔×éÓūĶعż²ā¶Øµ„Ī»Ź±¼äÄŚÉś³ÉCO2µÄĖŁĀŹ£¬Ģ½¾æijÖÖÓ°Ļģ»Æѧ·“Ó¦ĖŁĀŹµÄŅņĖŲ£¬Éč¼ĘŹµŃé·½°øČēĻĀ£ØKMnO4ČÜŅŗŅŃĖį»Æ£©£ŗ
| ŹµŃéŠņŗÅ | AČÜŅŗ | BČÜŅŗ |
| ¢Ł | 20mL 0.1mol•L﹣1 H2C2O4ČÜŅŗ | 30mL 0.01mol•L﹣1 KMnO4ČÜŅŗ |
| ¢Ś | 20mL 0.2mol•L﹣1 H2C2O4ČÜŅŗ | 30mL 0.01mol•L﹣1 KMnO4ČÜŅŗ |
£Ø1£©øĆŹµŃéĢ½¾æµÄŹĒ””””ŅņĖŲ¶Ō»Æѧ·“Ó¦ĖŁĀŹµÄÓ°Ļģ£®ĻąĶ¬Ź±¼äÄŚÕėĶ²ÖŠĖłµĆCO2µÄĢå»ż“󊔹ŲĻµŹĒ””””£¾””””£ØĢīŹµŃéŠņŗÅ£©£®
£Ø2£©ČōŹµŃé¢ŁŌŚ2minÄ©ŹÕ¼ÆĮĖ4.48mL CO2£Ø±ź×¼×“æöĻĀ£©£¬ŌņŌŚ2minÄ©£¬c£ØMnO4﹣£©=””””mol/L£®
£Ø3£©³żĶعż²ā¶ØŅ»¶ØŹ±¼äÄŚCO2µÄĢå»żĄ“±Č½Ļ·“Ó¦ĖŁĀŹ£¬±¾ŹµŃ黹æÉĶعż²ā¶Ø””Ą“±Č½Ļ»Æѧ·“Ó¦ĖŁĀŹ£®
£Ø4£©Š”×éĶ¬Ń§·¢ĻÖ·“Ó¦ĖŁĀŹ×ÜŹĒČēĶ¼¶ž£¬ĘäÖŠt1”«t2Ź±¼äÄŚĖŁ ĀŹ±äæģµÄÖ÷ŅŖŌŅņæÉÄÜŹĒ£ŗ¢ŁøĆ·“Ó¦·ÅČČ”¢¢Ś””””£®

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀĻĀ£¬ĻĀĮŠČÜŅŗµÄpH»ņĪ¢Į£µÄĪļÖŹµÄĮæÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | Ca£ØClO£©2ČÜŅŗÖŠ£ŗc£ØCa2+£©£¾c£ØClO﹣£©£¾c£ØOH﹣£©£¾c£ØH﹣£© |
| ”” | B£® | µČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄNa2SO3ČÜŅŗÓėNaHSO3ČÜŅŗ»ģŗĻ£ŗc£ØNa+£©=c£ØSO32﹣£©+c£ØHSO3﹣£©+c£ØH2SO3£© |
| ”” | C£® | ½«0.2mol£®L﹣1µÄijŅ»ŌŖĖįHAČÜŅŗŗĶ0.1mol£®L﹣1µÄNaOHČÜŅŗµČĢå»ż»ģŗĻŗóČÜŅŗµÄpH“óÓŚ7£¬Ōņ·“Ó¦ŗóµÄ»ģŗĻŅŗ£ŗ2c£ØOH﹣£©+c£ØA﹣£©=2c£ØH+£©+c£ØHA£© |
| ”” | D£® | ijČÜŅŗÖŠĖ®µēĄė³öµÄc£ØOH﹣£©=1”Į10﹣amol£®L﹣1Čōa£¾7Ź±£¬ŌņpHøĆČÜŅŗµÄŅ»¶ØĪŖ14﹣a |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com