
已知A、B、C、D之间的转化关系如图所示。下列说法正确的是
 A. 若A为Fe,D为氢气,则B一定为酸
A. 若A为Fe,D为氢气,则B一定为酸
B. 若A、D为化合物,B为水,则C一定是气体单质
C. 若A、B、C、D均为化合物,该反应一定属于复分解反应
D. 若A、B、C、D均为10电子微粒,且C是可使湿润的红色石蕊试纸变蓝的气体,则D常温下一定呈液态
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案科目:高中化学 来源: 题型:
《有机化学基础》
 Ⅰ(8分)双酚A (也称BPA)常用来生产防碎塑料聚碳酸酯。BPA的结构简式如右下图所示。
Ⅰ(8分)双酚A (也称BPA)常用来生产防碎塑料聚碳酸酯。BPA的结构简式如右下图所示。
(1)双酚A中的含氧官能团为 ▲ (填名称)。
(2)下列关于双酚A的叙述中,不正确的是 ▲ (填标号)。
A.遇FeCl3溶液变色
B.可以发生还原反应
C.1 mol双酚A最多可与2 mol Br2反应
D.可与NaOH溶液反应
(3)双酚A的一种合成路线如下图所示:

①丙烯→A的反应类型是 ▲ 。
②B→C的化学方程式是 ▲ 。
Ⅱ(7分)甲苯和溴乙烷混合物可通过如下流程进行分离。
 |
请填写下列空白:
(1)X的结构简式为 ▲ ;
(2)操作①能否用分液 ▲ ,理由是 ▲ 。
(3)写出甲苯与溴乙烷的混合物中加入试剂A时发生反应的化学方程式: ▲ 。
(4)如果Y为乙烯,则试剂B为 ▲ ,“一定条件”是指 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出下列反应的化学方程式:
①乙烯跟溴发生加成反应: ;
②苯跟溴在FeBr3催化剂下发生取代反应: ;
(2)写出下列反应的离子方程式:
③烧碱溶液吸收氯气: ;
④稀硝酸与铜片反应: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学──选修3:物质结构与性质] (15分)
CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等。已知:
|
2Cu2++2Cl-+SO2+2H2O===2CuCl↓+4H++SO42-
2CuCl2+SnCl2=2CuCl↓+SnCl4
②CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子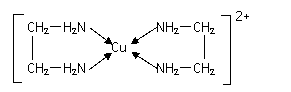

请回答下列问题:
(1)基态Cu原子的核外电子排布式为________________________,H、N、O三种元素的电负性由大到小的顺序是____________________。
(2)SO2分子的空间构型为______________,与SnCl4互为等电子体的一种离子的化学式为 。
(3)乙二胺分子中氮原子轨道的杂化类型为 ,乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的沸点高的多,原因是 。
(4)②中所形成的配离子中含有的化学键类型有 。(填字母)
A.配位键 B.极性键 C.离子键 D.非极性键
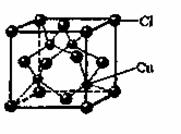 (5)CuCl的晶胞结构如上图所示,其中Cl原子的配位数为__ _________________。
(5)CuCl的晶胞结构如上图所示,其中Cl原子的配位数为__ _________________。
(6)若晶体的密度为ρg/cm3,阿伏加德罗常数用NA表示,则晶
胞内最远的两个Cu原子之间的距离是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,一定体积的CO、CO2和O2组成的混合气体,点燃后完全转化为CO2,恢复到原来状态时,体积变为90mL,则原混合气体的体积可能是
A.80mL B.100 mL C.150 mL D.145 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既不是氧化剂又不是还原剂等。下列反应与Br2 + SO2 + 2H2O H2SO4 + 2HBr相比较,水的作用不相同的是
A.2Na2O2 + 2H2O 4NaOH + O2↑ B.4Fe(OH)2 + O2 + 2H2O 4Fe(OH)3
C.2F2 + 2H2O 4HF + O2 D.C12 + H2O HC1 + HC1O
查看答案和解析>>
科目:高中化学 来源: 题型:
丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活。
已知:①2C3H8(g)+7O2(g)= 6CO(g)+8H2O(l);△H=-2741.8kJ/mol
②2CO(g) + O2(g) = 2CO2(g) ΔH=-566 kJ/mol
(1)反应C3H8(g)+5O2(g) = 3CO2(g)+4H2O(l)的△H=
(2)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:
CO(g)+ H2O(g) 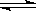 CO2(g)+ H2(g),ΔH>0
CO2(g)+ H2(g),ΔH>0
①下列事实能说明该反应达到平衡的是( )。
a.体系中的压强不发生变化 b.υ正(H2)=υ逆(CO )
c.混合气体的平均相对分子质量不发生变化 d.CO2的浓度不再发生变化
②在某温度下,反应物的起始浓度分别为:c(CO)= 1 mol·L-1, c(H2O)=2.4 mol·L-1; 达到平衡后,CO的转化率为60%,此时H2O的转化率为 ;
(3)CO2可用NaOH溶液吸收得到Na2CO3或NaHCO3。
①Na2CO3俗称纯碱,解释其水溶液呈碱性的原因,用离子方程式表示 ,
该溶液中离子浓度由大到小的顺序为 。
②0.1mol/L Na2CO3溶液中c(OH-)-c(H+)= [用含c(HCO-3)、c(H2CO3)的关系式表示]
查看答案和解析>>
科目:高中化学 来源: 题型:
相同体积的氯化钠、氯化镁、氯化铝溶液分别与过量的硝酸银溶液反应,所生成的沉淀物质的量相同,则原氯化钠、氯化镁、氯化铝溶液的物质的量浓度之比为( )
A.1 :2 :3 B.3 :2 :1 C.6 :3 :1 D.6 :3 :2
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示表示阿伏伽德罗常数的值,下列说法正确的是
A.1mol Na2O2粉末中含离子总数为4NA
B.22.4LCO2中含有的原子数为3NA
C.1mol单质钠在常温下或点燃条件下与O2完全反应转移的电子数都为NA
D.在一定量的稀硝酸中加入56g铁粉且完全溶解,转移的电子一定为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com