
核黄素又称维生素B2,可促进发育和细胞再生,有利于增进视力,减轻眼睛疲劳。核黄素分子的结构为:
已知: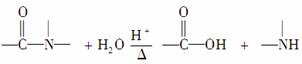 有关核黄素的下列说法中,不正确的是( )
有关核黄素的下列说法中,不正确的是( )
A.该化合物的分子式为C17H22N4O6
B.酸性条件下加热水解,有CO2生成
C.酸性条件下加热水解,所得溶液加碱后有NH3生成
D.能发生酯化反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
偏二甲肼与N2O4 是常用的火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2 (l )+2N2O4 (l )=2CO2 (g )+3N2 (g )+4H2O (l ) (Ⅰ)
(1)若将反应(Ⅰ)设计成原电池,则正极的电极反应式为
(酸性电解质)。
(2)火箭残骸中常现红棕色气体,原因为:N2O4 (g) 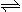 2NO2 (g) (Ⅱ)
2NO2 (g) (Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)为 (填“吸热”或“放热”)反应。
(3)一定温度下,反应(Ⅱ)的焓变为ΔH。现将1 mol N2O4 充入一恒压密闭容器中,
下列示意图正确且能说明反应达到平衡状态的是________.
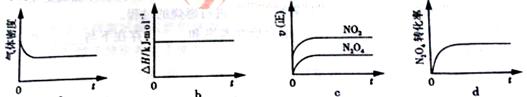
若在相同温度下,上述反应改在体积为1L的恒容密闭容器中进行,平衡常数________(填“增大”“不变”或“减小”),反应3s后NO2的物质的量为0.6mol,则0~3s内的平均反应速率v(N2O4)=________mol·L-1·s-1。
(4)NO2可用氨水吸收生成NH4NO3 。25℃时,将amol NH4NO3溶于水,溶液显酸性,原因是 (用离子方程式表示)。向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将______(填“正向”“不”或
“逆向”)移动,所滴加氨水的浓度为_______mol·L-1。(NH3·H2O的电离平衡常数
Kb=2×10—5 mol·L-1)
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH为2。下列对该溶液的叙述中,不正确的是( )
A.该温度高于25℃
B.由水电离出的[H+]=1.0×10-10 mol·L-1
C.加入NaHSO4晶体抑制了水的电离
D.该温度下加入等体积pH=12的NaOH溶液可使该溶液恰好呈中性
查看答案和解析>>
科目:高中化学 来源: 题型:
科学家预言,未来最理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)在适当的催化剂作用下水解成葡萄糖,再将葡萄糖转化为乙醇,用作燃料。
(1)写出由绿色植物秸秆转化为乙醇的化学方程式:
①________________________________________________________________________;
②________________________________________________________________________。
(2)乙醇还可用于合成其他有机物,如图是用乙醇为起始原料合成环状酯D的框图,请在方框内填入相应有机物的结构简式:
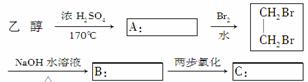
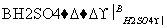
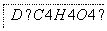
(3)写出B+C―→D的化学方程式:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是( )
A.组成蛋白质的氨基酸几乎都是α氨基酸
B.利用盐析可以分离和提纯蛋白质
C.DNA是生物体遗传信息的载体、蛋白质合成的模板
D.RNA主要存在于细胞核中,它根据DNA提供的信息控制体内蛋白质的合成
查看答案和解析>>
科目:高中化学 来源: 题型:
当氢氧化镁固体在水中达到溶解平衡Mg(OH)2(s)
 Mg2+(aq)+2OH-(aq)时,为使Mg(OH)2固体的量减少,须加入少量的( )
Mg2+(aq)+2OH-(aq)时,为使Mg(OH)2固体的量减少,须加入少量的( )
A.MgCl2 B.NaOH C.MgSO4 D.NaHSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
难溶电解质在水溶液中存在着电离平衡。在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数(Ksp)。例如:Cu(OH)2(s)
 Cu2+(aq)+2OH-,Ksp=[Cu2+]·[OH-]2=2×10-20 mol3·L-3。当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。
Cu2+(aq)+2OH-,Ksp=[Cu2+]·[OH-]2=2×10-20 mol3·L-3。当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解。
(1)某CuSO4溶液里[Cu2+]=0.02 mol·L-1,如要生成Cu(OH)2沉淀,应调整溶液的pH,使之大于________。
(2)要使0.2 mol·L-1 CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液pH为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对可逆反应aA(g)+bB(g)
 cC(g)+dD(g),达到平衡时,各物质的物质的量浓度应满足以下关系:
cC(g)+dD(g),达到平衡时,各物质的物质的量浓度应满足以下关系: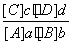 =K,K为一常数,称为化学平衡常数,其反应的K值只与温度有关,现有反应:CO(g)+H2O(g)
=K,K为一常数,称为化学平衡常数,其反应的K值只与温度有关,现有反应:CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH<0,在850℃时,K=1。
CO2(g)+H2(g) ΔH<0,在850℃时,K=1。
(1)若升高温度到950℃,达到平衡K________(填“大于”、“小于”或“等于”)1。
(2)850℃时,若向一容积可变的密闭容器中同时充入1.0 mol CO,3.0 mol H2O,1.0 mol CO2和x mol H2,则:
①当x=5.0时,上述平衡向________(填“正反应”或“逆反应”)方向移动。
②若要使上述反应开始时向正反应方向进行,则x应满足的条件是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
“烂版液”是制印刷锌版时,用稀硝酸腐蚀锌版后得到的“废液”(含有少量的Cl-、Fe3+)。某化学兴趣小组拟用“烂版液”制取Zn(NO3)2·6H2O的过程如下:

已知:Zn(NO3)2·6H2O是一种无色晶体,水溶液呈酸性,Zn(NO3)2能与碱反应,得到的产物具有两性。
(1)“烂版液”中溶质的主要成分是______(填化学式,下同)。
(2)在操作①中保持pH=8的目的是
________________________________________________________________________。
(3)沉淀Ⅰ的主要成分是____________。
(4)操作③中加热煮沸的目的是________________;此步操作的理论依据是
________________________________________________________________________。
(5)操作④保持pH=2的目的是____________;此步操作中所用的主要仪器是
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com