
(1)今有2H2+O2 2H2O反应,构成燃料电池,则电极反应式为:负极____________________、正极__________________。
2H2O反应,构成燃料电池,则电极反应式为:负极____________________、正极__________________。
(2)如把H2改为甲烷,KOH做导电物质,则负极电极反应式为_____________
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 化合物M是某种解热镇痛药,以A为原料的工业合成路线如下图所示:
化合物M是某种解热镇痛药,以A为原料的工业合成路线如下图所示:
|
 已知:
已知:

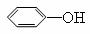 ① +
① +  + CH3COOH
+ CH3COOH

完成下列填空:
写出反应类型: 反应① 反应③ 。
A结构简式: 。由A合成D至少需要 个步骤才能完成。
写出反应④的化学方程式:
。
B的有苯环结构的同分异构体中有一种能在NaOH(aq)中发生水解。1mol该有机物最多消耗NaOH mol。写出满足下列条件所有的F的同分异构体的结构简式:
①是一种芳香族化合物; ②属α-氨基酸; ③苯环上有4种不同环境的氢原子
。 由 B不能一步完成,请解释可能的原因。
由 B不能一步完成,请解释可能的原因。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH),以下说法中不正确的是
A.甲醇分子内C原子的杂化方式为sp3杂化
B.甲醇分子内的O—C—H键角大于甲醛分子内的O—C—H键角
C.甲醛分子内C原子上无孤对电子
D.甲醛分子两个C—H键夹角小于120°
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关滴定操作的顺序正确的是
①用标准溶液润洗滴定管②往滴定管内注入标准溶液③检查滴定管是否漏水④滴定⑤洗涤
A. ⑤①②③④ B. ③⑤①②④
C. ⑤②③①④ D. ②①③⑤④
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:

下列叙述不正确的是
A. 放电时负极反应为:Zn - 2e— + 2OH— == Zn(OH)2
B. 充电时阳极反应为:Fe(OH)3 -3e— + 5OH— == FeO42— + 4H2O
C. 放电时每转移3moL电子,正极有1 mol K2FeO4被氧化
D. 放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学原理的应用,主要是利用沉淀溶解平衡原理来解释的是( )
①灰粪共用损肥分;②使用含氟牙膏能生成更难溶且耐酸的氟磷酸钙对牙齿起到更好的保护作用③溶洞、珊瑚的形成;④水垢中Mg(OH)2的形成;⑤误将钡盐[BaCl2、Ba(NO3)2]当做食盐食用后,常用0.5%的Na2SO4溶液解毒;
A.① ② ③ ④ B.② ③ ⑤ C.② ③ ④ ⑤ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A.NH4HSO3溶液与过量的NaOH溶液混合:NH4++OH- ==-NH3·H2O
B.Na2SO3溶液使酸性KMnO4溶液褪色:5SO32- + 6H+ + 2MnO4- == 5SO42- + 2Mn2+ +3H2O
C.向Na2CO3溶液中加入过量CH3COOH溶液 CO32-+2H+== CO2↑+H2O
D.Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I- = 2Fe2++I2
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用白云石制备高纯氧化镁的工艺流程如下:

已知白云石的主要成分可表示为:
CaO 32.50%;MgO 20.58%;Fe2O3 2.18%;SiO2 0.96%;其他 43.78%
(1)为了提高白云石的煅烧效果,可以采取的措施是 ▲ 。
若在实验室中煅烧白云石,需要的仪器除酒精灯、三脚架以外,还需要 ▲ 。
A.蒸发皿 B.坩埚 C.泥三角 D.石棉网
(2)加入H2SO4控制pH时,终点pH对产品的影响如图8所示,pH过高会导致镁浸率降低,其原因为 ▲ ,pH过低对产品影响是 ▲ 。


(3)从溶液中获得CaSO4·2H2O的操作是蒸发浓缩、 ▲ 、过滤、洗涤、干燥。
(4)写出沉淀反应中的离子方程式: ▲ 。
检验沉淀是否洗净的方法是: ▲ 。
(5)沉淀反应过程中,温度对产品的纯度也有一定的影响。图9为反应温度对氧化镁纯度的影响。最终确定本反应的适宜温度为 ▲
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com