
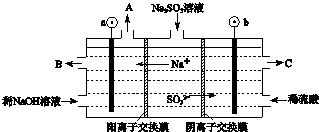
·ÖĪö £Ø1£©SO2ŌŚŃĢ³¾µÄ“ß»ÆĻĀŠĪ³ÉĮņĖįŹĒ2SO2+2H2O+O2=2H2SO4£»
£Ø2£©¢Łøł¾ŻČż¶ĪŹ½Ēó³ö×Ŗ»ÆĮ棬ŌŁøł¾Ż·“Ó¦ĖŁĀŹµÄ¶ØŅåŹ½¼ĘĖć£»
¢Ś»ÆŃ§Ę½ŗāµÄ±źÖ¾ŹĒÕżÄę·“Ó¦ĖŁĀŹĻąĶ¬£¬ø÷×é·Öŗ¬Įæ±£³Ö²»±ä£»
£Ø3£©¢Łøł¾Żµē½ā³ŲÖŠŅõŃōĄė×ÓµÄŅĘ¶Æ·½Ļņ£ŗŃōĄė×ÓŅĘĻņŅõ¼«æÉŅŌÅŠ¶Ļ¢ŁĶ¼ÖŠa¼«ŅŖĮ¬½ÓµēŌ“µÄøŗ¼«£¬SO32-ŌŚŃō¼«Ź§Č„µē×Ó±ä³ÉSO42-£¬ĖłŅŌCæŚĮ÷³öµÄĪļÖŹŹĒH2SO4£»¢ŚSO32-Ź§Č„µē×Ó±»Ńõ»Æ³ÉSO42-£»
¢Ūµē½ā¹ż³ĢÖŠŅõ¼«Ēų·ÅĒāÉś¼ī£¬Ė®±äĪŖĒāŃõ»ÆÄĘ£¬Ņõ¼«Ēų±ä»ÆµÄÖŹĮæµČÓŚĒāŃõ»ÆÄʵÄÖŹĮæ¼õČ„ĻūŗÄĖ®µÄÖŹĮ棻
øł¾Żµē×ÓŹŲŗć¼ĘĖć£ŗ
2e-”«Na2SO3”«2H2O”«2NaOH”«Ņõ¼«Ēų±ä»ÆµÄÖŹĮæ
126g 36g 80g 44g
12.6g x
x=4.4g£¬ÓÉ“Ė½ā“š£®
½ā“š ½ā£ŗ£Ø1£©SO2ŌŚŃĢ³¾µÄ“ß»ÆĻĀŠĪ³ÉĮņĖįŹĒ2SO2+2H2O+O2=2H2SO4£¬¹Ź“š°øĪŖ£ŗ2SO2+2H2O+O2=2H2SO4£»
£Ø2£©¢ŁT1ĪĀ¶ČŹ±£¬ŌŚ2LµÄĆܱÕČŻĘ÷ÖŠ¼ÓČė4.0molSO2ŗĶ2.0molO2£¬5minŗó·“Ó¦“ļµ½Ę½ŗā£¬¶žŃõ»ÆĮņµÄ×Ŗ»ÆĀŹĪŖ50%£¬
2SO2£Øg£©+O2?2SO3£Øg£©”÷H£¼0
ĘšŹ¼Įæ£Ømol£© 2.0 1.0 0
±ä»ÆĮæ£Ømol£©2.0”Į50% 0.5 0.5
Ę½ŗāĮæ£Ømol£© 1.0 0.5 0.5
Ē°5minÄŚO2µÄĘ½¾ł·“Ó¦ĖŁĀŹ=$\frac{0.5mol}{2L”Į5min}$=0.05mol/£ØL•min£©£»
¹Ź“š°øĪŖ£ŗ0.05mol/£ØL•min£©£»
¢Ś»ÆŃ§Ę½ŗāµÄ±źÖ¾ŹĒÕżÄę·“Ó¦ĖŁĀŹĻąĶ¬£¬ø÷×é·Öŗ¬Įæ±£³Ö²»±ä£»
a£®ĪļÖŹµÄÅØ¶Č¹ŲĻµŗĶĘšŹ¼ĮæŗĶ×Ŗ»ÆĀŹÓŠ¹Ų£¬SO2”¢O2”¢SO3ČżÕßµÄÅضČÖ®±ČĪŖ2£ŗ1£ŗ2 ²»ÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹Źa²»·ūŗĻ£»
b£®ŅņĪŖøĆ·“Ó¦ĪŖĘųĢåĪļÖŹµÄĮæŌö“óµÄ·“Ó¦£¬ŗćĪĀŗćČŻĢõ¼žĻĀ£¬Ń¹ĒæĪŖ±äĮ棬µ±ČŻĘ÷ÖŠĘųĢåµÄŃ¹Ēæ²»±äĖµĆ÷“ļµ½Ę½ŗāדĢ¬£¬¹Źb·ūŗĻ£»
c£®·“Ó¦Ē°ŗóĘųĢåÖŹĮæ²»±ä£¬ČŻĘ÷Ģå»ż²»±ä£¬ĆܶČŌŚ·“Ó¦¹ż³ĢÖŠŗĶĘ½ŗāדĢ¬¶¼²»±ä£¬ČŻĘ÷ÖŠ»ģŗĻĘųĢåµÄĆܶȱ£³Ö²»±ä²»ÄÜĖµĆ÷·ŃÓĆ“ļµ½Ę½ŗāדĢ¬£¬¹Źc²»·ūŗĻ£»
d£®SO3µÄĪļÖŹµÄĮæ²»ŌŁ±ä»Æ£¬ÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹Źd·ūŗĻ£»
e£®SO2µÄÉś³ÉĖŁĀŹŗĶSO3µÄÉś³ÉĖŁĀŹĻąµČĖµĆ÷ÕżÄę·“Ó¦ĖŁĀŹĻąĶ¬£¬ÄÜĖµĆ÷·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬¹Źe·ūŗĻ£»
¹Ź“š°øĪŖ£ŗbde£»
£Ø3£©¢Łøł¾Żµē½ā³ŲÖŠŅõŃōĄė×ÓµÄŅĘ¶Æ·½Ļņ£ŗŃōĄė×ÓŅĘĻņŅõ¼«æÉŅŌÅŠ¶Ļ¢ŁĶ¼ÖŠa¼«ŅŖĮ¬½ÓµēŌ“µÄøŗ¼«£¬SO32-ŌŚŃō¼«Ź§Č„µē×Ó±ä³ÉSO42-£¬ĖłŅŌCæŚĮ÷³öµÄĪļÖŹŹĒH2SO4£¬
¹Ź“š°øĪŖ£ŗøŗ£»ĮņĖį£»
¢ŚSO32-Ź§Č„µē×Ó±»Ńõ»Æ³ÉSO42-£¬µē¼«·“Ó¦Ź½ĪŖ£ŗSO32--2e-+H2O=SO42-+2H+£¬¹Ź“š°øĪŖ£ŗSO32--2e-+H2O=SO42-+2H+£»
¢Ūµē½ā¹ż³ĢÖŠŅõ¼«Ēų·ÅĒāÉś¼ī£¬Ė®±äĪŖĒāŃõ»ÆÄĘ£¬Ņõ¼«Ēų±ä»ÆµÄÖŹĮæµČÓŚĒāŃõ»ÆÄʵÄÖŹĮæ¼õČ„ĻūŗÄĖ®µÄÖŹĮ棻
øł¾Żµē×ÓŹŲŗć£ŗ
2e-”«Na2SO3 ”«2H2O”«2NaOH”«Ņõ¼«Ēų±ä»ÆµÄÖŹĮæ
126g 36g 80g 44g
12.6g x
x=4.4g
ČōĻūŗÄ12.6g Na2SO3£¬ŌņŅõ¼«Ēų±ä»ÆµÄÖŹĮæĪŖ4.4 g£¬¹Ź“š°øĪŖ£ŗ4.4g£®
µćĘĄ ±¾Ģāæ¼²éĮĖ»Æѧ·“Ó¦ĖŁĀŹµÄ¼ĘĖć”¢»ÆŃ§Ę½ŗāµÄÅŠ¶Ļ”¢µē»ÆѧµČ£¬ŹŌĢā²ąÖŲ¶Ōѧɜ»ł“”ÖŖŹ¶µÄѵĮ·ŗĶ¼ģŃ飬ӊĄūÓŚĢįøßѧɜĮé»īŌĖÓĆĖłŃ§ÖŖŹ¶½ā¾öŹµ¼ŹĪŹĢāµÄÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ°²»ÕŹ”øßŅ»ÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ijČÜŅŗÖŠŗ¬ÓŠ“óĮæµÄCl£”¢CO32-”¢SO42-µČČżÖÖŅõĄė×Ó”£Čē¹ūֻȔŅ»“ĪøĆČÜŅŗ¾ĶÄܹ»·Ö±š½«ČżÖÖŅõĄė×ÓŅĄ“Ī¼ģŃé³öĄ“£¬ĻĀĮŠŹµŃé²Ł×÷Ė³ŠņÕżČ·µÄŹĒ
¢ŁµĪ¼ÓHNO3ČÜŅŗ ¢Ś¹żĀĖ ¢ŪµĪ¼ÓAgNO3ČÜŅŗ ¢ÜµĪ¼ÓBa(NO3)2ČÜŅŗ”£
A£® ¢Ł¢Ü¢Ś¢Ū B£® ¢Ü¢Ś¢Ł¢Ū C£® ¢Ū¢Ś¢Ł¢Ü D£® ¢Ü¢Ś¢Ū¢Ś¢Ł
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģ½ĖÕŹ”øßČżÉĻµŚŅ»“Ī²āŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ČēĶ¼ŹĒ½šŹōĆ¾ŗĶĀ±ĖŲµ„ÖŹ(X2)·“Ó¦µÄÄÜĮæ±ä»ÆŹ¾ŅāĶ¼”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
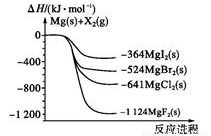
A£®ÓÉMgCl2ÖĘČ”MgŹĒ·ÅČČ¹ż³Ģ
B£®ČČĪČ¶ØŠŌ£ŗMgI2<MgBr2<MgCl2<MgF2
C£®³£ĪĀĻĀŃõ»ÆŠŌ£ŗF2£¼Cl2£¼Br2£¼I2
D£®ÓÉĶ¼æÉÖŖ“ĖĪĀ¶ČĻĀMgBr2(s)ÓėCl2(g)·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖ£ŗ
MgBr2(s)£«Cl2(g)=MgCl2(s)£«Br2(g)£¬¦¤H£½£117kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĶʶĻĢā
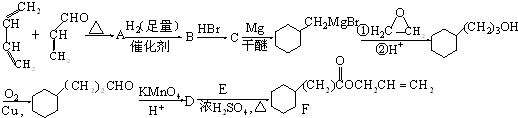
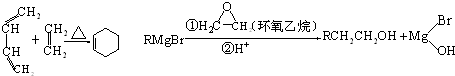
 £¬AÖŠĖłŗ¬¹ŁÄÜĶŵÄĆū³ĘŹĒČ©»ł”¢Ģ¼Ģ¼Ė«¼ü£®
£¬AÖŠĖłŗ¬¹ŁÄÜĶŵÄĆū³ĘŹĒČ©»ł”¢Ģ¼Ģ¼Ė«¼ü£® £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¾ŪŅŅĻ©ĖÜĮĻµÄĄĻ»ÆŹĒÓÉÓŚ·¢ÉśĮĖ¼Ó³É·“Ó¦ | |
| B£® | ±½ÖŠŗ¬ÓŠĢ¼Ģ¼Ė«¼ü£¬ĘäŠŌÖŹøśŅŅĻ©ĻąĖĘ | |
| C£® | ŅŅĻ©Ź¹äåĖ®ĶŹÉ«ŗĶ±½ÓėäåĖ®»ģŗĻÕńµ“ŗóĖ®²ć±äĪŖĪŽÉ«ŌĄķĻąĶ¬ | |
| D£® | £ØNH4£©2SO4ÅØČÜŅŗŗĶCuSO4ČÜŅŗ¶¼ÄÜŹ¹µ°°×ÖŹ³ĮµķĪö³ö |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | BÓėAÖ»ÄÜ×é³ÉBA3»ÆŗĻĪļ | |
| B£® | C”¢D”¢EŠĪ³ÉµÄ»ÆŗĻĪļÓėĻ”ĮņĖįæÉÄÜ·¢ÉśŃõ»Æ»¹Ō·“Ó¦ | |
| C£® | A”¢B”¢CŠĪ³ÉµÄ»ÆŗĻĪļŅ»¶Ø²»ÄÜ·¢ÉśĖ®½ā | |
| D£® | EµÄŃõ»ÆĪļŅ»¶ØÓŠĒæµÄŃõ»ÆŠŌ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŗĖµēŗÉŹż | B£® | ÖŹ×ÓŹż | C£® | ÖŠ×ÓŹż | D£® | µē×ÓŹż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com