
【题目】下表为元素周期表的一部分。
碳 | 氮 | Y | |
X | 硫 | Z |
回答下列问题
(1)Z元素在周期表中的位置为__________。
(2)元素周期表中与Z元素同周期原子半径最大的是(写元素名称)__________,其最高价氧化物对应的水化物含有的化学键类型____________。
(3)下列事实能说明Y元素的非金属性比硫元素的非金属性强的是___;
a.Y单质与H2S溶液反应,溶液变浑浊
b.在氧化还原反应中,1molY单质比1molS得电子多
c.Y和S两元素的简单氢化物受热分解,前者的分解温度高
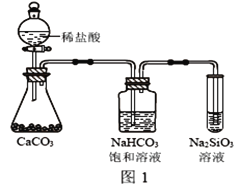
(4)根据下图实验,可以证明碳的非金属性比X强。饱和小苏打溶液的作用__________。发生的离子方程式是:__________________
(5)重水(D2O)是重要的核工业原料,下列说法错误的是________。
a.氘(D)原子核内有1个中子
b.1H与D互称同位素
c.H2O与D2O互称同素异形体
d.1H218O与D216O的相对分子质量相同
【答案】第三周期ⅦA族 钠 离子键和(极性)共价键 ac 除去挥发出来的HCl气体 H++HCO3-=H2O+CO2↑ c
【解析】
根据元素在周期表的位置关系可知,X与碳同族,位于碳的下一周期,应为Si元素;Y与硫元素同族,位于硫的上一周期,应为O元素;Z与硫元素处于同一周期,位于第VIIA族,应为Cl元素,结合元素原子的结构和元素周期律分析作答。
(1)Z为Cl,质子数为17,电子结构有3个电子层,最外层电子数为7;
(2)电子层相同时核电荷数越大离子半径越小,即同一周期元素原子的半径从左到右依次减小;根据化学键与物质类别分析;
(3)Y元素的非金属性比S元素的非金属性强,可利用单质之间的置换反应、氢化物稳定性比较;
(4)利用碳酸钙与稀盐酸反应制备二氧化碳,利用饱和碳酸氢钠溶液除去二氧化碳中的HCl气体,再将二氧化碳通入硅酸钠溶液中出现白色胶状沉淀,以此证明碳酸的酸性比硅酸强;
(5)a.原子的中子数等于质量数-质子数;
b.具有相同质子数、不同中子数的原子互为同位素;
c.同种元素形成的不同单质互为同素异形体;
d.D即是2H,据此分析。
(1)Z为Cl元素,在周期表中的位置为第三周期ⅦA族;
(2)根据上述分析可知,与Cl处于同一周期的原子半径最大的是钠,其最高价氧化物对应的水化物为氢氧化钠,其化学键类型为:离子键和(极性)共价键,故答案为:钠;离子键和(极性)共价键;
(3)a. Y单质与H2S溶液反应,溶液变浑浊,则Y的得到电子能力强,Y的非金属性强,a项正确;
b. 在氧化还原反应中,1mol Y单质比1mol S得电子多,得电子多少不能比较非金属性,b项错误;
c. Y和S两元素的简单氢化物受热分解,前者的分解温度高,可知Y的氢化物稳定,则Y的非金属性强,c项正确;
故答案为:ac;
(4)图中实验装置中,制备二氧化碳的过程中会有HCl气体挥发,为除去二氧化碳气体中的HCl,证明碳酸的酸性比硅酸强,需用饱和碳酸氢钠溶液进行除杂,发生的离子方程式为:H++HCO3-=H2O+CO2↑,故答案为:除去挥发出来的HCl气体;H++HCO3-=H2O+CO2↑;
(5)a. 氘(D)原子内有1个质子,质量数为2,因此中子数=2-1=1,a项正确;
b. 1H与D具有相同质子数、不同中子数,二者互称同位素,b项正确;
c. H2O与D2O均为水,属于化合物,不是单质,不能互称同素异形体,c项错误;
d. D即是2H,所以1H218O与D216O的相对分子质量相同,d项正确;
故答案为:c。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、W均为中学常见的纯净物,它们之间有如下转化关系(其它产物及反应条件已略去,反应可以在水溶液中进行)![]() :A
:A![]() B
B![]() C;
C;
Ⅰ.若A为有刺激性气味的气体,水溶液呈碱性;C为红棕色气体,与水反应生成一元强酸D,D具有强氧化性。
(1)在催化剂作用下,A与C反应可生成两种无污染物质,该反应化学方程式为_______。
(2)工业上常用过量的Na2CO3溶液吸收C,生成等物质的量的两种硝酸盐,该反应的离子方程式为___。
Ⅱ.若A、C、W都是常见气体,C是导致酸雨的主要气体,常温下A与C反应生成B,则该反应的化学方程式为_____。
某化学活动小组将搜集到的一定量的酸雨保存在密闭容器中,每隔一定时间测酸雨的pH,发现在起始一段时间内,酸雨的pH呈减小趋势,用离子方程式解释原因:________。
Ⅲ.A、B、C三种物质的溶液均显碱性,焰色反应均为黄色;C常作面包和糕点的发泡剂,受热分解可生成B。若将标准状况下2.24L的W通入150mL1 molL-1 的A溶液中,充分反应。总反应的离子方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物命名正确的是 ( )
A. ![]() 2—乙基丙烷B. CH3CH2CH2CH2OH 1—丁醇
2—乙基丙烷B. CH3CH2CH2CH2OH 1—丁醇
C. ![]() 邻二甲苯D. CH2=C(CH3)2 2—甲基—2—丙烷
邻二甲苯D. CH2=C(CH3)2 2—甲基—2—丙烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是_________(填“吸热”或“放热”)反应,NO2和CO的总能量_________(填“小于”、 “大于”或“等于”)CO2和NO的总能量。
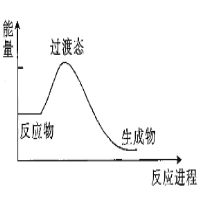
(2)在某体积为2L的密闭容器中充入0.5mol NO2和1mol CO,在一定条件下发生反应:NO2+COCO2+NO,2min时,测得容器中NO的物质的量为0.2mol,则:
①该段时间内,用CO2表示的平均反应速率为_________。
②假设此反应在5min时达到平衡,则此时容器内气体的总物质的量为_________。
③下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是_________。
A.容器内气体的质量保持不变
B.NO2的物质的量浓度不再改变
C.NO2的消耗速率与CO2的消耗速率相等
D.容器内气体总的物质的量保持不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有五种元素,其中A、B、C为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
A元素的核外电子数和电子层数相等 |
B元素原子的核外p电子数比s电子数少1 |
C原子第一至第四电离能如下: I1=738 kJ·mol-1,I2=1451 kJ·mol-1,I3=7733 kJ·mol-1,I4=10540 kJ·mol-1 |
F是前四周期中电负性最小的元素 |
G在周期表的第八列 |
(1)已知BA5为离子化合物,写出其电子式:________。
(2)B元素基态原子中能量最高的电子,其电子云在空间有______个方向,原子轨道呈____形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为![]() ,该同学所画的电子排布图违背了___________________________________。
,该同学所画的电子排布图违背了___________________________________。
(4)G位于第____族____区,该元素的核外电子排布式为_____________________。该二价离子很容易被氧化成三价离子,从原子轨道理论解释原因________________________
(5)检验F元素的方法是___,请用原子结构的知识解释产生此现象的原因: ______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成防晒霜的主要成分E的一种路线图如下:
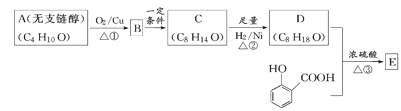
已知:2RCH2CHO![]()
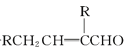
请按要求回答下列问题:
(1)D的官能团结构简式为____________________
(2)反应③的反应类型为__________。
(3)反应①的化学方程式:____________________
(4)E的结构简式:____________________。
(5)A的同分异构体有多种,写出其中核磁共振氢谱吸收峰面积之比为1∶9的结构简式:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的结构简式为 CH2=CH-C≡C![]() ,下列有关其几何结构的说法正确的是( )
,下列有关其几何结构的说法正确的是( )
A. 所有碳原子不可能在同一平面上 B. 有4个碳原子在同一直线上
C. 有5个碳原子在同一直线上 D. 有6个碳原子在同一直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)有机物![]() 的系统名称是_______________________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是__________________。
的系统名称是_______________________,将其在催化剂存在下完全氢化,所得烷烃的系统名称是__________________。
(2)苯的同系物中,有的侧链能被酸性高锰酸钾溶液氧化,生成芳香酸,反应如下:(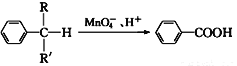 R、R′表示烷基或氢原子),但若侧链上直接与苯环连接的原子上没有C—H键,则不容易被氧化。
R、R′表示烷基或氢原子),但若侧链上直接与苯环连接的原子上没有C—H键,则不容易被氧化。
①现有苯的同系物甲和乙,分子式都是C10H14。甲不能被酸性高锰酸钾溶液氧化为芳香 酸,它的结构简式是________________________;
②有机物丙也是苯的同系物,分子式也是C10H14,它的苯环上的一溴代物只有一种。丙的结构简式共有四种,写出其余三种: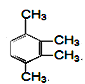 __________、_________________、______________
__________、_________________、______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】初中化学常见物质A-I分别是下列物质中的一种:锌、氢氧化钠、硫酸铜溶液、稀盐酸、碳酸钠溶液、石灰水、生石灰、石灰石和水。他们之间相互的反应(每种物质只能用一次)恰好包含了化合反应(A+B)、分解反应(C)、置换反应(D+E)、中和反应(F+G)、复分解反应(H+I)等反应类型。试回答下列问题:
(1)A+B的反应化学方程式是______________________。
(2)C的化学式为___________;硫酸铜溶液参加___________反应(填反应类型)。
(3)H+I的反应方程式是_________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com