
【题目】材料的不断发展可以促进社会进步。 完成下列填空:
(1) “玉兔”号月球车开创了我国月球表面探索的先河,其制备材料中使用了镁铝合金,选用镁铝合金的优点是____________________。(任写一点)
(2)光导纤维简称“光纤”,是一种由玻璃制成、能传输光线、结构特殊的玻璃纤维。现在家中的电话线和网线大都采用光纤线。光纤的主要成分是二氧化硅,二氧化硅的晶体类型是____________________。(单选)
a.金属晶体 b.离子晶体 c.原子晶体 d.分子晶体
(3)随着我国经济的快速发展,对电池新材料需求的不断增加,再加上手机、笔记本电脑、数码相机、摄像机、汽车等产品对新型、高效、环保电池材料的强劲需求,我国电池新材料市场将不断扩大。而铜锌原电池是一种最基本的将化学能转变为电能的装置,其中铜作________极,锌作_________极。
(4)塑料制品作为一种新型材料,具有质轻、防水、耐用、生产技术成熟、成本低的优点,在全世界被广泛应用且呈逐年增长趋势。乙烯通过加聚反应可以制成聚乙烯塑料,请写出聚乙烯的结构简式____________________。
科目:高中化学 来源: 题型:
【题目】利用CO和H2在催化剂的作用下合成甲醇,发生的反应如下:CO(g)+2H2(g)![]() CH3OH(g),在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
CH3OH(g),在体积一定的密闭容器中按物质的量之比1:2充入CO和H2,测得平衡混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。下列说法正确的是
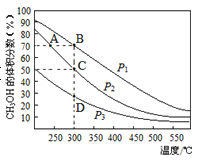
A. 该反应的△H<0,且p1<p2
B. 反应速率:ν逆(状态A)>ν逆(状态B)
C. 在C点时,CO转化率为75%
D. 在恒温恒压条件下向密闭容器中充入不同量的CH3OH,达平衡时CH3OH的体积分数也不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室通常用图所示的装置来制取氨气。请按要求回答下列问题:

(1)实验室制取氨气的化学反应方程式为__。
(2)除了以上方法。下面也能用于制备氨气的是___。
①固态氯化铵加热分解
②浓氨水中加入固体氢氧化钠
③加热浓氨水
(3)NH3的催化氧化的化学反应方程式为__。
(4)①用装置A收集氨气时,应选择氨气的进气口是___(选填“a”或“b”),并说明选择的理由___。
②打开装置A中的止水夹,若观察到烧瓶内产生了红色喷泉,则说明氨气具有的性质是___、___。

(5)通常可以用什么方法来检验无色溶液中是否有NH4+___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请用下图所示仪器装置设计一个包括电解饱和食盐水并测定电解时产生的氢气的体积和检验氯气的氧化性的实验装置。其中A是金属Fe,B是石墨电极。
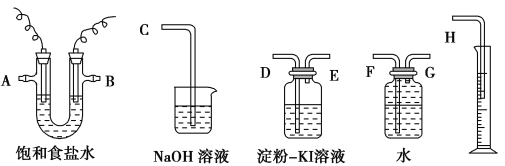
(1)所选仪器连接时,各接口的顺序是(填各接口的代号字母):A接______,________接______,B接________,________接________。
(2)实验时,装置中的石墨电极接电源的________极,所发生的电极反应式为_____________;铁电极接电源的________极,所发生的电极反应式为___________;
此电解总反应的离子方程式为________________________________。
(3)实验测得产生的氢气体积(已折算成标准状况)为5.60 mL,电解后溶液的体积恰好为50.0 mL,则溶液中OH—的浓度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种“氢氧化锶-氯化镁法”制备“牙膏用氯化锶(SrCl2·6H2O)”的工艺流程如图:

(1)锶与钙同主族。金属锶应保存在__中(填“水”、“乙醇”或“煤油”)。
(2)天青石(主要成分SrSO4)经过多步反应后可制得工业碳酸锶。其中第一步是与过量焦炭隔绝空气微波加热还原为硫化锶,该过程的化学方程式为___。
(3)工业碳酸锶中含有CaCO3、MgCO3、BaCO3等杂质。“滤渣”的主要成分是___。
(4)“重结晶”时蒸馏水用量[以质量比m(H2O):m(SrO)表示]对Sr(OH)2·8H2O纯度及产率的影响如下表。最合适的质量比为___,当质量比大于该比值时,Sr(OH)2·8H2O产率减小,其原因是___。
质量mH2O:mSrO | 4:1 | 5:1 | 6:1 | 7:1 | 8:1 | 9:1 | 10:1 |
Sr(OH)2·8H2O纯度% | 98.64 | 98.68 | 98.65 | 98.64 | 98.63 | 98.63 | 98.65 |
Sr(OH)2·8H2O产率% | 17.91 | 53.36 | 63.50 | 72.66 | 92.17 | 89.65 | 88.93 |
(5)水氯镁石是盐湖提钾后的副产品,其中SO42-含量约为1%,“净化”过程中常使用SrCl2除杂,写出该过程的离子方程式___
(6)若需进一步获得无水氯化锶,必须对SrCl2·6H2O(M=267g·mol-1)进行脱水。脱水过程采用烘干法在170℃下预脱水,失重达33.7%,此时获得的产物化学式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.原子序数之差为2的两种元素不可能位于同一主族
B.D-核外有36个电子 ,则元素D位于第四周期第ⅦA族
C.位于同一主族相邻的甲、乙两种元素,甲的原子序数为![]() ,则乙的原子序数可能为
,则乙的原子序数可能为![]()
D.位于同一周期的甲、乙两种元素,甲位于第IIA族,原子序数为![]() ,乙位于第ⅢA族,则乙原子序数可能为
,乙位于第ⅢA族,则乙原子序数可能为![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水开发利用的部分过程如图所示。下列说法正确的是( )
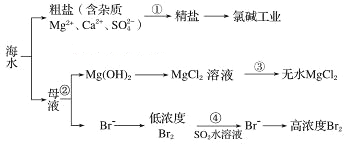
A. 过程①中,粗盐的提纯只涉及除杂、结晶等物理过程
B. 过程②中,工业上常用 NaOH 作为沉淀剂得到 Mg(OH)2
C. 过程③中,直接加热蒸干 MgCl2 溶液即可得到无水 MgCl2
D. 过程④中,可以选用 Na2SO3 饱和溶液来代替 SO2 水溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、磷、硫等元素形成的单质和化合物在生活、生产中有重要的用途。
(1)下列氮原子的电子排布图表示的状态中,能量由低到高的顺序是___(填字母)。
A.![]() B.
B.![]()
C.![]() D.
D.![]()
(2)P4S3可用于制造火柴,其分子结构如图所示:

①P4S3分子中硫原子的杂化轨道类型为___。
②1molP4S3分子中含有的孤电子对的数目为___对。
(3)科学家合成了一种阳离子“N5n+”,其结构是对称的,5个N排成“V”形,每个N都达到8电子稳定结构,且含有2个氮氮三键,此后又合成了一种含有“N5n+”的化学式为“N8”的离子晶体(该晶体中每个N原子都达到了8电子稳定结构),N8的电子式为___。(CN)2中键与键之间的夹角为180°,并有对称性,分子中每个原子的最外层均满足8电子稳定结构,其结构式为___。
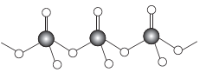
(4)直链多磷酸根阴离子是由两个或两个以上磷氧四面体通过共用顶角氧原子连接起来的,其结构如图所示。则由n个磷氧四面体形成的这类磷酸根离子的通式为___。
(5)碳酸盐中的阳离子不同,热分解温度就不同。下表为四种碳酸盐的热分解温度和对应金属阳离子的半径。随着金属阳离子半径的增大,碳酸盐的热分解温度逐渐升高,原因是___。
碳酸盐 | MgCO3 | CaCO3 | SrCO3 | BaCO3 |
热分解温度/℃ | 402 | 900 | 1172 | 1360 |
金属阳离子半径/pm | 66 | 99 | 112 | 135 |
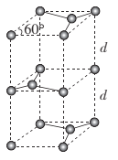
(6)石墨的晶胞结构如图所示。已知石墨的密度为ρg·cm-3,C-C键的键长为rcm,NA为阿伏加德罗常数的值,则石墨晶体的层间距d=___cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列图示所得出的结论正确的是( )
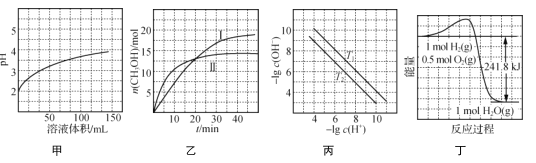
A. 图甲表示1 mL pH=2某一元酸溶液加水稀释时,pH随溶液总体积的变化曲线,说明该酸是强酸
B. 图乙表示恒容密闭容器中其他条件相同时改变温度,反应CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ
CH3OH(g)+H2O(g)中n(CH3OH)随时间的变化曲线,说明反应平衡常数KⅠ>KⅡ
C. 图丙表示不同温度下水溶液中-lg c(H+)、-lg c(OH-)变化曲线,说明T1>T2
D. 图丁表示1 mol H2和0.5 mol O2反应生成1 mol H2O过程中的能量变化曲线,说明H2的燃烧热是241.8 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com