
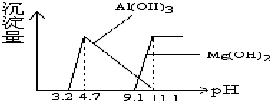
 根据Al(OH)3 的Ksp=1.3×10-33、Mg(OH) 2的Ksp=5.6×10-12,等物质的量浓度AlCl3、MgCl2混合溶液与NaOH溶液反应生成相应沉淀,pH与沉淀量关系如下图:
根据Al(OH)3 的Ksp=1.3×10-33、Mg(OH) 2的Ksp=5.6×10-12,等物质的量浓度AlCl3、MgCl2混合溶液与NaOH溶液反应生成相应沉淀,pH与沉淀量关系如下图:| A. | Al(OH)3 和Mg(OH)2在水溶液中的电离过程完全相同 | |
| B. | 若改变溶液的pH,在pH<4.7时,n(Mg2+)几乎不变化 | |
| C. | 当pH>11.1时,溶液中只有NaCl和NaAlO2(Na[Al(OH)4]) | |
| D. | 等物质的量浓度Al3+、Mg2+混合溶液与氨水反应生成相应沉淀,氨水的pH与沉淀量关系与上图相似 |
分析 A.氢氧化铝为两性氢氧化物,在溶液中存在酸式和碱式电离;
B.根据图象可知,pH小于4.7时镁离子还没有开始沉淀;
C.溶液中还存在过量的氢氧化钠;
D.氨水为弱碱,不会溶解氢氧化铝.
解答 解:A.Al(OH)3 为类型氢氧化物,在溶液中能够电离出氢离子,还能够电离出氢氧根离子,而Mg(OH)2在水溶液中只能电离出氢氧根离子,所以二者的电离过程不完全相同,故A错误;
B.由图象可知,pH≥9.1时开始生成氢氧化镁沉淀,所以pH<4.7时,n(Mg2+)几乎不变化,故B正确;
C.当pH>11.1时,溶液中含有NaCl、NaAlO2(Na[Al(OH)4])及过量的NaOH,故C错误;
D.等物质的量浓度Al3+、Mg2+混合溶液与氨水反应生成相应沉淀,由于氨水为弱碱,不会溶解氢氧化铝,所以氨水的pH与沉淀量关系与上图不同,故D错误;
故选B.
点评 本题考查了难溶物溶解平衡及其影响,题目难度中等,明确溶解平衡及其影响因素为解答关键,注意氨水为弱碱,不会溶解氢氧化铝,为易错点,试题培养了学生的灵活应用能力.


科目:高中化学 来源:2016-2017学年天津市高二上9月调研化学试卷(解析版) 题型:选择题
在一定温度下的定容密闭容器中,当物质的下列物理量不再发生变化时,表明反应A(s)+2B(g) C(g)+D(g)已达到平衡状态的是( )
C(g)+D(g)已达到平衡状态的是( )
A.混合气体的密度 B.混合气体的总物质的量
C.混合气体的压强 D.混合气体的总体积
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液的pH | B. | 醋酸的电离平衡常数 | ||
| C. | 溶液的导电能力 | D. | 醋酸的电离程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
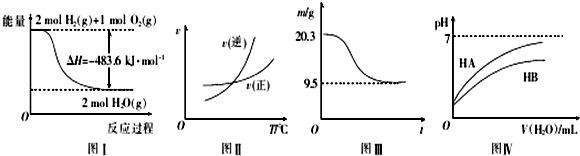
| A. | 图I表示H2与O2发生反应过程中的能量变化,则H2的燃烧热△H=-241.8 kJ.mol-1 | |
| B. | 图Ⅱ表示某可逆反应正、逆反应速率随温度的变化,则该反应的正反应是放热反应 | |
| C. | 图Ⅲ表示0.1 mol MgCl2•6H2O在空气中充分加热时固体质量随时间的变化 | |
| D. | 图Ⅳ表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH大于同浓度NaB溶液的pH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸 | HClO2 | HF | HCN | H2S |
| Ka | 1×10-2 | 6.3×10-4 | 4.9×10-10 | K1=9.1×10-8K2=1.1×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com