
【题目】某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其核电荷数,请你根据下面的提示做出自己的判断。
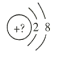
(1)若该微粒是电中性微粒,这种微粒的元素符号是___。
(2)若该微粒的还原性很弱,失去1个电子后变为原子,该原子的单质氧化性很强,该单质与水反应的化学方程式为___。
(3)若该微粒的氧化性很弱,得到1个电子后变为原子,该原子的单质还原性很强,该单质在氧气中燃烧所得产物的化学式为___。
(4)若该微粒的还原性很弱,失去2个电子后变成原子,其氢化物的结构式为___。
【答案】Ne 2F2+2H2O=4HF+O2 Na2O2 H—O—H或H—O—O—H
【解析】
按相应粒子的性质推测元素并按要求回答;
(1)由该单核微粒的结构示意图可知,其核外有10个电子,若该微粒是电中性微粒,由核电荷数=核外电子数可知,这种微粒是Ne原子;答案为:Ne;
(2)若该微粒的还原性很弱,失去1个电子后变为原子,说明该元素的原子含有9个电子,为F元素,F2和水反应生成HF和O2,化学方程式为![]() ;答案为:2F2+2H2O=4HF+O2;
;答案为:2F2+2H2O=4HF+O2;
(3)若该微粒的氧化性很弱,得到1个电子后变为原子,说明该元素的原子含有11个电子,为Na元素,Na在氧气中燃烧生成Na2O2;答案为:Na2O2;
(4)若该微粒的还原性很弱,失去2个电子后变成原子,说明该元素的原子含有8个电子,为O元素,O元素的氢化物是H2O或H2O2,结构式为H—O—H或H—O—O—H;答案为:H—O—H或H—O—O—H。


科目:高中化学 来源: 题型:
【题目】常温时,用![]() 滴定
滴定![]() 某一元酸HX,滴定过程中pH变化曲线如图所示。
某一元酸HX,滴定过程中pH变化曲线如图所示。
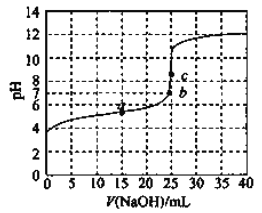
下列说法正确的是
A. HX溶液显酸性的原因是![]()
B. 点a,![]()
C. 点b,![]() 与
与![]() 恰好完全反应
恰好完全反应
D. 点c,![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各离子①H+ ②Cl- ③Al3+ ④K+ ⑤S2- ⑥OH- ⑦NO3- ⑧NH4+中,不影响水的电离平衡的是( )
A.①③⑤⑦⑧B.②④⑦C.①⑥D.②④⑥⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度、相同浓度的六种溶液,其pH由小到大的顺序如图所示,图中①②③代表的物质可能分别是
![]()
A.NH4Cl (NH4)2SO4 CH3COONa
B.(NH4)2SO4 NH4Cl CH3COONa
C.(NH4)2SO4 NH4Cl NaOH
D.CH3COOH NH4Cl (NH4)2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积固定为2L的密闭容器中,充入![]() 和
和![]() ,在温度
,在温度![]() 时发生反应,
时发生反应,![]() ,
,![]() 的浓度随时间变化如图,下列说法正确的是
的浓度随时间变化如图,下列说法正确的是![]()
![]()
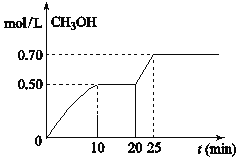
A.从开始到25分钟,![]() 的转化率是
的转化率是![]()
B.从20分钟到25分钟,可能是缩小容器体积
C.其它条件不变,将温度升到![]() ,平衡常数增大
,平衡常数增大
D.从反应开始到10分钟,![]() 的平均反应速率
的平均反应速率![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用反应: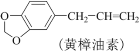
![]()
![]()
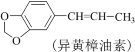
![]() 合成洋茉莉醛的流程如图所示。下列说法错误的是( )
合成洋茉莉醛的流程如图所示。下列说法错误的是( )

A.水洗的目的是除去KOH
B.试剂X应选用有机溶剂
C.黄樟油素和异黄樟油素互为同分异构体
D.进行蒸馏操作时可选用球形冷凝管
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a~n10中元素在周期表中的位置如图所示,请回答下列问题:
a | ||||||||
b | c | d | e | |||||
f | g | h | m | n | ||||
…… |
(1)m的阴离子的结构示意图为___。
(2)b的最高价氧化物的化学式为___;用化学方程式表示f、d的单质形成f2d2的过程___。
(3)d、g、n形成的简单离子的半径由大到小的顺序为___(用离子符号表示)。
(4)以上元素组成的物质有下列框图中的转化关系,其中甲为10电子微粒。
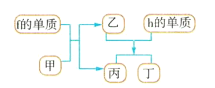
请写出h的单质与乙反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D四种元素的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8。A原子的L层电子数与K、M层电子数之和相等,D原子的K、L层电子数之和等于其电子总数的一半。
请回答下列问题:
(1)四种元素的元素符号依次是A________B________C________D________。它们的原子半径由大到小的顺序是________________(用元素符号表示)。
(2)试写出四种元素的简单离子结构示意图A________B________C________D________。它们的离子半径由大到小的顺序是________________(用元素符号表示)
(3)A、B、C、D的最高价氧化物对应水化物的化学式分别是________________,分别比较其最高价氧化物对应水化物酸性和碱性的强弱________________。
(4)写出其中非金属元素形成的气态氢化物的化学式:________,其稳定性强弱是_________,理由是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表是元素周期表的一部分,请用元素符号、离子符号或相关化学式回答有关问题:
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)表中能形成两性氢氧化物的元素在周期表中的位置是________;
(2)写出②的气态氢化物的结构式________;
(3)元素④⑤⑥⑦离子半径由大到小的顺序________;
(4)①、⑥、⑦三种元素的最高价氧化物的水化物中酸性最强的是________;④、⑤、⑨三种元素的最高价氧化物的水化物中碱性最强的是
(5)⑦和⑩氧化性较强的是________用一个置换反应证实这一结论(写化学方程式)___________________________。
(6)④⑤两元素相比较,金属性较强的是________,可以验证该结论的实验是________;
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将形状、大小相同的这两种元素的单质用砂纸打磨后分别和同浓度的盐酸反应
(c)将形状、大小相同两种元素的单质用砂纸打磨后分别和热水作用,并滴入酚酞
(d)比较这两种元素的气态氢化物的稳定性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com