
下列离子方程式书写不正确的是
A.单质铜与稀硝酸反应:Cu + 2 H+ + 2 NO3- ==Cu2+ + 2 NO↑+ H2O
B.NaOH溶液与足量的Ca(HCO3)2溶液反应:2HCO3- + 2OH- + Ca2+==CaCO3↓+ 2H2O
C.等物质的量的FeBr2和Cl2在溶液中的反应:2Fe2+ + 2Br - + 2Cl2==2Fe3+ + Br2 + 4Cl -
D.氨水吸收少量的二氧化硫:2NH3·H2O + SO2==2NH4+ +SO32- + H2O
科目:高中化学 来源: 题型:
用硝酸、硫酸、盐酸、醋酸、钠盐、钾盐、钡盐相互反应,符合离子方程式2H++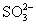 ====H2O+SO2↑的反应个数有( )
====H2O+SO2↑的反应个数有( )
A.4个 B.5个
C.8个 D.12个
查看答案和解析>>
科目:高中化学 来源: 题型:
已知X、Y是主族元素,I为电离能,单位是kJ·mol-1。请根据下表所列数据判断,错误的是
| 元素 | I1 | I2 | I3 | I4 |
| X | 500 | 4600 | 6900 | 9500 |
| Y | 580 | 1800 | 2700 | 11600 |
A.元素X的常见化合价是+1 B.元素Y是ⅢA族元素
C.元素X与氯形成化合物时,化学式可能是XCl
D.若元素Y处于第三周期,它可与冷水剧烈反应
查看答案和解析>>
科目:高中化学 来源: 题型:
 已知A、B、C、D、E、F、G都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素。A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子,G的+1价阳离子正好充满K、L、M三个电子层。回答下列问题:
已知A、B、C、D、E、F、G都是周期表中前四周期的元素,它们的核电荷数依次增大,其中A、B、C、D、E为不同主族的元素。A、C的最外层电子数都是其电子层数的2倍,B的电负性大于C,透过蓝色钴玻璃观察E的焰色反应为紫色,F的基态原子中有4个未成对电子,G的+1价阳离子正好充满K、L、M三个电子层。回答下列问题:
(1)A、B、C、D、E、F、G几种元素中第一电离能最小的是___________ (填元素符号),D元素的原子核外有 种不同运动状态的电子;有 种不同能级的电子。基态的F3+核外电子排布式是 。
(2)B的气态氢化物在水中的溶解度远大于A、C的气态氢化物,原因是
。
(3)化合物AC2的电子式是 。
 (4)FD3与ECAB溶液混合,得到含多种配合物的血红色溶液,其中配位数为5的配合物的化学式是 。
(4)FD3与ECAB溶液混合,得到含多种配合物的血红色溶液,其中配位数为5的配合物的化学式是 。
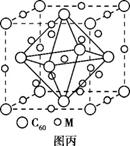
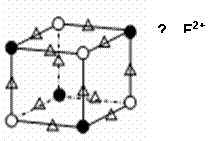
(5)化合物EF是一种蓝色晶体,右图
表示其晶胞的1/8(E+未画出)。该蓝色晶体
的一个晶胞中E+的个数为 。
(6)G的二价阳离子能与乙二胺(H2N—CH2一CH2一NH2)形成配离子:该配离子中含有的化学键类型有 。(填字母)
a.配位键 b.极性键 c.离子键 d.非极性键
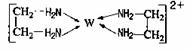
阴离子CAB-中的A原子与乙二胺(H2N—CH2一CH2一NH2)中C原子的杂化方式分别为 和 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
A.L2+与R2-的核外电子数相等
B.M与T形成的化合物既能与酸反应又能与强碱反应
C.氢化物的稳定性为H2T<H2R
D.单质与浓度相等的稀盐酸反应的速率为Q>L
查看答案和解析>>
科目:高中化学 来源: 题型:
下列示意图与对应的反应情况正确的是
A B C D
A.含0.01molKOH 和0.01mol Ca(OH)2 的混合溶液中缓慢通入CO2
B.KAl(SO4)2溶液中逐滴加入Ba(OH)2 溶液
C. n(O2)=1mol时,高温下C和O2在密闭容器中的反应产物
D.n(NaOH)=1mol时,CO2和NaOH溶液反应生成的盐
查看答案和解析>>
科目:高中化学 来源: 题型:
下列属于氧化还原反应的是( )
A.SO2+H2O====H2SO3
B.H2CO3====CO2↑+H2O
C.2NaOH+H2SO4====Na2SO4+2H2O
D.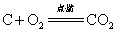
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中反应A(g)+2B(g) C(g)分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100 mol·L-1,c(B)=0.200 mol·L-1,c(C)=0 mol·L-1。反应物A的浓度随时间的变化如图所示。
C(g)分别在三种不同实验条件下进行,它们的起始浓度均为c(A)=0.100 mol·L-1,c(B)=0.200 mol·L-1,c(C)=0 mol·L-1。反应物A的浓度随时间的变化如图所示。
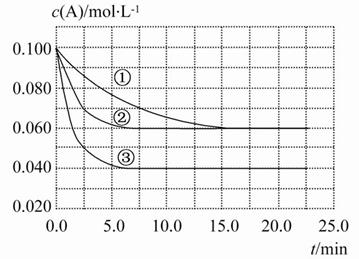
下列说法正确的是( )
A.若反应①、②的平衡常数分别为K1、K2,则K1<K2
B.反应A+2B C的ΔH>0
C的ΔH>0
C.实验②平衡时B的转化率为60%
D.减小反应③的压强,可以使平衡时c(A)=0.060 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
SO2是常见的大气污染物之一,下列措施中能够减少SO2排放量的是( )
①用天然气代替煤炭作民用燃料
②使用水煤气或干馏煤气作燃料
③硫酸厂使用V2O5作催化剂,加快SO2的转化速率
④将块状煤粉碎,提高其燃烧效率
⑤在煤中加入生石灰后燃烧
⑥循环处理吸收塔放出的尾气
A.①②③④⑤ B.①③⑤⑥ C.①②⑤⑥ D.②③④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com