
| A. | C3H8(l)+5O2(g)═3CO2(g)+4H2O(l)△H=-2219.9 kJ/mol | |
| B. | 2CO(g)+O2(g)═2CO2(g)△H=-566.0 kJ/mol | |
| C. | H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8 kJ/mol | |
| D. | 2C(s)+O2(g)═2CO(g)△H=-221 kJ/mol |
分析 燃烧热规定了可燃物的物质的量为1mol,完全燃烧生成稳定的化合物即C→CO2(g),H→H2O(l),对应热化学方程式中可燃物的化学计量数为1,据此分析.
解答 解:A、燃烧热规定了可燃物的物质的量为1mol,完全燃烧生成稳定的化合物即C→CO2(g),H→H2O(l),故A正确;
B、燃烧热规定了可燃物的物质的量为1mol,对应热化学方程式中可燃物的化学计量数为1,故B错误;
C、燃烧热规定了可燃物的物质的量为1mol,完全燃烧生成稳定的化合物即H→H2O(l),故C错误;
D、燃烧热规定了可燃物的物质的量为1mol,对应热化学方程式中可燃物的化学计量数为1,故D错误;
故选A.
点评 本题考查化学反应能量知识,题目难度不大,注意正确理解燃烧热的概念.


科目:高中化学 来源: 题型:选择题
| A. | 滤液中一定有Fe2(SO4)3和FeSO4 | |
| B. | 滤液中可能有CuSO4,一定有FeSO4、ZnSO4 | |
| C. | 滤渣中一定有Cu和Fe,一定无Zn | |
| D. | 滤渣中可能有Cu、Fe和Zn |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
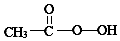 )常用作纺织品漂白剂.
)常用作纺织品漂白剂.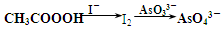
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应前后的气体质量之比一定是1:3 | |
| B. | 两种单质X、Y的摩尔质量之比是1:3 | |
| C. | 在生成物Z中,X的质量分数为50% | |
| D. | Z中X、Y两元素的原子个数比为3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 50g | B. | 60mol/g | C. | 60g/mol | D. | 50g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
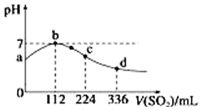 标准状况下,向100mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图中曲线所示.下列分析正确的是( )
标准状况下,向100mL H2S饱和溶液中通入SO2气体,所得溶液pH变化如图中曲线所示.下列分析正确的是( )| A. | b点水的电离程度比c点水的电离程度大 | |
| B. | 氢硫酸的酸性比亚硫酸的酸性强 | |
| C. | 原H2S溶液的物质的量浓度为0.05 mol•L-1 | |
| D. | a点对应溶液的导电性比d点强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu(OH)2中加入硫酸:OH-+H+=H2O | |
| B. | 钠加入水中:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 铁片与氯化铜溶液反应:Fe+Cu2+=Cu+Fe2+ | |
| D. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++OH-+H++SO42-=H2O+BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com