
| n |
| V |
| 0.15mol |
| 0.2L |
|


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
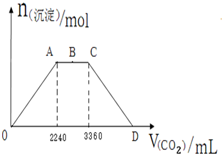 向KOH和Ca(OH)2的混合稀溶液中通入CO2,生成沉淀的物质的量(n)和通入CO2的体积(V)关系如图所示.已知B位于A、C中点.
向KOH和Ca(OH)2的混合稀溶液中通入CO2,生成沉淀的物质的量(n)和通入CO2的体积(V)关系如图所示.已知B位于A、C中点.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢铵和硝酸铵 |
| B、碳酸铵和硝酸铵 |
| C、氯化铵和碳酸氢铵 |
| D、氯化铵和碳酸铵 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验序号 | 样品的质量/g | NaOH 溶液的体积/ml | 氨气的体积/L |
| Ⅰ | 7.4 | 40.00 | 1.68 |
| Ⅱ | 14.8 | 40.00 | 3.36 |
| Ⅲ | 22.2 | 40.00 | 1.12 |
| Ⅳ | 37.0 | 40.00 | 0.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①②④ |
| C、③④⑤ | D、①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 实验方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为Na2O |
| 方案2 | ①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的BaCl2溶液 | 出现白色沉淀 | |
| ②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com