
【题目】下列说法正确的是
A.符号3px所代表的含义是第三个电子层px轨道有3个伸展方向
B.能层数为3时,有3s、3p、3d三个轨道
C.氢原子中只有1个电子,故氢原子核外只有1个轨道
D.s能级的原子轨道半径与能层序数有关
科目:高中化学 来源: 题型:
【题目】图中所示实验装置用于研究温度对凝乳酶催化乳汁凝固的影响。

先将酶和乳汁分别加入2个试管,然后将两个试管放入同一水浴环境中持续15min,再将酶和乳汁倒入同一试管中混合,保温并记录凝乳所需要的时间。通过多次实验,记录在不同温度下凝乳所需要的时间,结果如下表:
装置 | A | B | C | D | E | F |
水浴温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 |
凝乳时间(min) | 很长 | 7.0 | 4.0 | 1.5 | 4.0 | 不凝固 |
(1)解释以下两种处理对实验结果的影响。
①将装置A中的混合物加温至40℃,乳汁凝固时间如何变化? ,原因是 。
②将装置F中的混合物冷却至40℃,乳汁凝固时间如何变化? ,原因是 。
(2)若将酶和乳汁先混合再进行F组实验,实验结果会不准确,原因是 。
(3)根据表格简要写出探究该酶催化作用的最适温度的实验思路 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关基本营养物质的说法中,正确的是( )
A. 糖类、油脂、蛋白质都是由C、H、O三种元素组成的高分子化合物
B. 淀粉遇KI溶液变蓝
C. 纤维素在人体内最终水解为葡萄糖
D. 蔗糖和麦芽糖互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F均为周期表中前四周期元素,其原子序数依次增大,其中A、B、C为短周期非金属元素。A是形成化合物种类最多的元素;B原子基态电子排布中只有一个未成对电子;C是同周期元素中原子半径最小的元素;D的基态原子在前四周期元素的基态原子中单电子数最多;E与D相邻,E的某种氧化物X与C的氢化物的浓溶液加热时反应常用于实验室制取气态单质C;F与D的最外层电子数相等。
回答下列问题(相关回答均用元素符号表示):
(1)D的基态原子的核外电子排布式是______________。
(2)B的氢化物的沸点比C的氢化物的沸点________(填“高”或“低”),原因是______________________。
(3)A的电负性________(填“大于”或“小于”)C的电负性,A形成的氢化物A2H4中A的杂化类型是________。
(4) X在制取C单质中的作用是________,C的某种含氧酸盐常用于实验室中制取氧气,此酸根离子中化学键的键角________(填“>”“=”或“<”)109°28′。
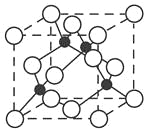
(5)已知F与C的某种化合物的晶胞结构如图所示,则该化合物的化学式是__________________,若F与C原子最近的距离为a cm,则该晶体的密度为________g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数的数值为NA)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】孔雀石主要成分是Cu2(OH)2CO3,还含少量FeCO3及Si的化合物,实验室以孔雀石为原料制备硫酸铜晶体的步骤如下:

(1)步骤Ⅰ中涉及的主要反应用离子方程式表示为_____.
(2)步骤Ⅱ中试剂①是_____(填代号).
a.KMnO4 b.H2O2 c.Fe粉 d.KSCN
(3)步骤Ⅲ加入CuO的目的是_____.
(4)步骤Ⅳ获得硫酸铜晶体,需要经过_____、_____、过滤等操作.
(5)孔雀石与焦炭一起加热可以生成Cu及其它无毒物质,写出该反应的化学方程式_____.
(6)测定硫酸铜晶体(CuSO4xH2O)中结晶水的x值:称取2.41g硫酸铜晶体,在____(填实验仪器名称)中加热至质量不再改变时,称量粉末的质量为1.6g.则计算得x=_____(计算结果精确到0.1).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝分别与足量的稀盐酸和氢氧化钠溶液反应,当两个反应放出的气体在相同状况下体积相等时,反应中消耗的HCl和NaOH的物质的量之比为 ( )
A.1∶1 B.2∶1 C.3∶1 D.1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚锡(SnSO4)是一种重要的硫酸盐,主要用于电镀工业的镀锡、铝合金表面的氧化着色、印染工业的媒染剂、双氧水去除剂等。某研究小组设计SnSO4制备路线如下:

查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成难溶物Sn(OH)Cl(碱式氯化亚锡)。
III.Sn(OH)2的性质与Al(OH)3性质相似。请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,这样操作的原因是。
(2)反应Ⅰ得到沉淀是SnO,得到该沉淀的离子方程式是。
(3)将反应I滤液中的溶质提取出来的操作是,滤液I溶质的成分是。
(4)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是。
(5)称取SnSO4·xH2O晶体50.2g,在隔绝空气的情况下小火加热至结晶水全部失去,冷却称量固体质量为43g,则该晶体的化学式为。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com