
 Z+W
Z+W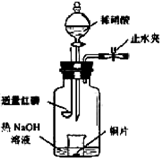
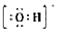 (2)2NH3(l) ? NH
(2)2NH3(l) ? NH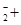 NH
NH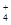
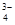 +3H2O
+3H2O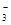 =3Cu2++2NO
=3Cu2++2NO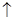 +4H2O
+4H2O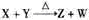 ,可知X为NH4+,Y为OH-,Z为NH3;故Y的电子式为:
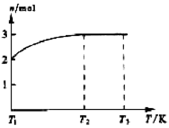
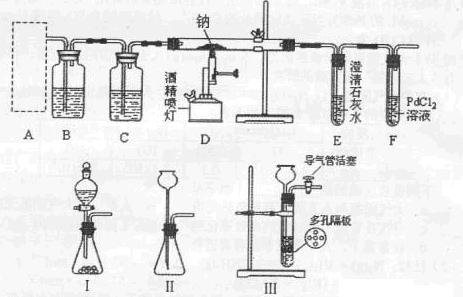
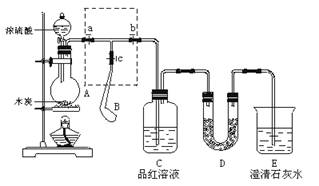
,可知X为NH4+,Y为OH-,Z为NH3;故Y的电子式为: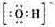 ,液氨电离和水相似,其电离式为:2NH3(l)=NH4++NH2-;用图示装置制备NO并验证其还原性,故整个操作中没有验证步骤,可以在制备到NO后,通入少量氧气,通过现象变化确定其还原性,故在c步骤中增加,打开止水夹,通入少量氧气;红磷充分燃烧生成P2O5,其余氢氧化钠反应为: P2O5+6OH-=2PO43-+3H2O,步骤c滴入硝酸后的现象为:Cu片逐渐溶解,有无色气泡产生,溶液由无色变为蓝色,反应为:3Cu+8H++2NO3-=3Cu2++2NO+4H2O;1molN2O4置于密闭容器中,升温过程中,逐渐转变为红棕色,说明N2O4=2NO2,此时装置中为2molNO2,根据图像中表示的意义,继续加压时,气体的物质的量增多,且为无色,超T2温度后,物质的量约为3mol,故其反应式为:2NO2=O2+2NO,其相对分子质量为:30.7。
,液氨电离和水相似,其电离式为:2NH3(l)=NH4++NH2-;用图示装置制备NO并验证其还原性,故整个操作中没有验证步骤,可以在制备到NO后,通入少量氧气,通过现象变化确定其还原性,故在c步骤中增加,打开止水夹,通入少量氧气;红磷充分燃烧生成P2O5,其余氢氧化钠反应为: P2O5+6OH-=2PO43-+3H2O,步骤c滴入硝酸后的现象为:Cu片逐渐溶解,有无色气泡产生,溶液由无色变为蓝色,反应为:3Cu+8H++2NO3-=3Cu2++2NO+4H2O;1molN2O4置于密闭容器中,升温过程中,逐渐转变为红棕色,说明N2O4=2NO2,此时装置中为2molNO2,根据图像中表示的意义,继续加压时,气体的物质的量增多,且为无色,超T2温度后,物质的量约为3mol,故其反应式为:2NO2=O2+2NO,其相对分子质量为:30.7。

科目:高中化学 来源:不详 题型:填空题
 .Na202 b.Na2C03 c.NaHCO3 d.Na2C03和C
.Na202 b.Na2C03 c.NaHCO3 d.Na2C03和C查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 实验目的 | 实验步骤及现象 |
| A | 检验Fe(NO3)2试样是否变质 | 试样加水溶解,加盐酸酸化,加KSCN溶液,出现血红色 |
| B | 检验某卤代烃是否是氯代烃 | 试样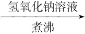 冷却 冷却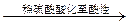 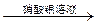 出现白色沉淀 出现白色沉淀 |
| C | 证明酸性条件H2O2氧化性比I2强 | NaI溶液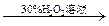 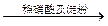 溶液变蓝色 溶液变蓝色 |
| D | 除去氯化钠晶体中少量硝酸钾 | 试样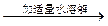 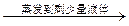   重结晶 重结晶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 5CO2+11H2O+2K2SO4+4MnSO4
5CO2+11H2O+2K2SO4+4MnSO4
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
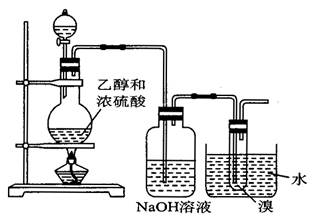
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com