
”¾ĢāÄæ”æijӊ»ś»ÆŗĻĪļAµÄĻą¶Ō·Ö×ÓÖŹĮæ(·Ö×ÓĮæ)“óÓŚ110£¬Š”ÓŚ150”£¾·ÖĪöµĆÖŖ£¬ĘäÖŠĢ¼ŗĶĒāµÄÖŹĮæ·ÖŹżÖ®ŗĶĪŖ52.24%£¬ĘäÓąĪŖŃõ”£Ēė»Ų“š£ŗ
(1)øĆ»ÆŗĻĪļ·Ö×ÓÖŠŗ¬ÓŠ___________øöŃõŌ×Ó”£
(2)øĆ»ÆŗĻĪļµÄ·Ö×ÓŹ½ĪŖ____________”£
(3)øĆ»ÆŗĻĪļ·Ö×ÓÖŠ×ī¶ąŗ¬______øöĢ¼ŃõĖ«¼ü”£
”¾“š°ø”æ4 C5H10O4 1
”¾½āĪö”æ
£Ø1£©ÓÉĢāŅāÖŖ£¬ŃõµÄÖŹĮæ·ÖŹżĪŖ1-52.24%=47.76%£¬ÓÉÓŠ»ś»ÆŗĻĪļµÄĻą¶Ō·Ö×ÓÖŹĮæ“óÓŚ110£¬Š”ÓŚ150£¬¼“·Ö×ÓÖŠŃõŌ×ÓøöŹżĪŖ“óÓŚ![]() =3.28£¬Š”ÓŚ
=3.28£¬Š”ÓŚ![]() =4.48£¬ĖłŅŌŃõŌ×ÓĪŖ4øö£»
=4.48£¬ĖłŅŌŃõŌ×ÓĪŖ4øö£»
£Ø2£©·Ö×ÓÖŠŃõŌ×ÓĪŖ4øö£¬ĖłŅŌC”¢HµÄĻą¶ŌŌ×ÓÖŹĮæÖ®ŗĶĪŖ£ŗ134-16”Į4=70£¬CŌ×Ó×ī“óŹżÄæ=![]() =5”10£¬¹Ź·Ö×ÓÖŠŗ¬ÓŠ5øöCŌ×Ó”¢10øöHŌ×Ó£¬æÉČ·¶Ø»ÆѧŹ½ĪŖC5H10O4£»
=5”10£¬¹Ź·Ö×ÓÖŠŗ¬ÓŠ5øöCŌ×Ó”¢10øöHŌ×Ó£¬æÉČ·¶Ø»ÆѧŹ½ĪŖC5H10O4£»
£Ø3£©C5H10O4Óė5øöCŌ×ӵı„ŗĶŃÜÉśĪļ£ØæɱķŹ¾ĪŖC5H12On£©±Č½ĻæÉÖŖ£¬·Ö×ÓÖŠ×ī¶ąŗ¬ÓŠ1øöōŹ»ł¹ŁÄÜĶÅ£¬¼“×ī¶ąŗ¬1øöĢ¼ŃõĖ«¼ü”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æøł¾ŻĪļÖŹ½į¹¹ÓŠ¹ŲŠŌÖŹŗĶĢŲµć£¬»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ti»łĢ¬Ō×ÓŗĖĶāµē×ÓÅŲ¼Ź½ĪŖ _____»łĢ¬ĀĮŌ×ÓŗĖĶāµē×ÓŌĘŠĪדӊ_________£ØĢīĆū³Ę£©”£
£Ø2£©±ūĻ©ėę£ØCH2=CH-CN£©·Ö×ÓÖŠ¦Į¼üŗĶ![]() ¼üµÄøöŹż±ČĪŖ_____,·Ö×ÓÖŠĢ¼Ō×Ó¹ģµĄµÄŌÓ»ÆĄąŠĶŹĒ___
¼üµÄøöŹż±ČĪŖ_____,·Ö×ÓÖŠĢ¼Ō×Ó¹ģµĄµÄŌÓ»ÆĄąŠĶŹĒ___
£Ø3£©Š“³öÓėNH4+»„ĪŖµČµē×ÓĢåµÄŅ»ÖÖ·Ö×ÓŗĶŅ»ÖÖĄė×ӵĻÆѧŹ½______”¢_______”£
£Ø4£©īŃ“ęŌŚĮ½ÖÖĶ¬ĖŲŅģ¹¹Ģ壬![]() ²ÉÄÉĮł·½×īĆܶѻż£¬
²ÉÄÉĮł·½×īĆܶѻż£¬![]() ²ÉÄÉĢåŠÄĮ¢·½¶Ń»ż£¬¼ų±šĮ½ÖÖīŃ¾§ĢåæÉŅŌÓĆ_____·Ø£¬ÓÉ
²ÉÄÉĢåŠÄĮ¢·½¶Ń»ż£¬¼ų±šĮ½ÖÖīŃ¾§ĢåæÉŅŌÓĆ_____·Ø£¬ÓÉ![]() ×Ŗ±äĪŖ
×Ŗ±äĪŖ![]() ¾§ĢåĢå»ż_____£ØĢī”°ÅņÕĶ”±»ņ”°ŹÕĖõ”±£©”£
¾§ĢåĢå»ż_____£ØĢī”°ÅņÕĶ”±»ņ”°ŹÕĖõ”±£©”£
£Ø5£©“¦ÓŚŅ»¶ØæÕ¼äŌĖ¶ÆדĢ¬µÄµē×ÓŌŚŌ×ÓŗĖĶā³öĻÖµÄøÅĀŹĆÜ¶Č·Ö²¼æÉÓĆ____________ŠĪĻó»ÆĆčŹö”£
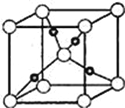
£Ø6£©CuÓėOŌŖĖŲŠĪ³ÉµÄijÖÖ»ÆŗĻĪļµÄ¾§°ū½į¹¹ČēĶ¼ĖłŹ¾£¬¾§°ūÖŠŃõŌ×ÓµÄÅäĪ»ŹżĪŖ____£¬Čō°¢·üŁ¤µĀĀŽ³£ŹżĪŖNA£¬¾§°ūµÄ±ß³¤ĪŖa pm,øĆ¾§ĢåµÄĆܶČĪŖ__gcm©3£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŌøÉŗ£“ųĪŖŌĮĻĢįČ”µāµ„ÖŹŗĶĀČ»Æ¼ŲµÄ¹ż³ĢÖ÷ŅŖ·ÖČż²½£ŗĶź³ÉĻĀĮŠĢīæÕ£ŗ
(1)²½ÖčŅ»£ŗ×ĘÉÕøÉŗ£“ų£¬Ź¹Ęä»Ņ»ÆŗóÓĆČČĖ®½žÅŻ”¢¹żĀĖ£¬ÖʵĆŌĮĻŅŗ£¬ŗ¬ÓŠĀČ»Æ¼ŲµČĪļÖŹ”£ŹµŃéŹŅ×ĘÉÕŗ£“ųÓ¦·ÅŌŚ____(ĢīŠ“ŅĒĘ÷Ćū³Ę)ÖŠ¼ÓČČ£¬Ń”ÓĆČČĖ®¶ų²»ŹĒĄäĖ®½žÅŻŗ£“ų»ŅµÄÄæµÄŹĒ____”£
(2)²½Ö趞£ŗŌĮĻŅŗ¾½į¾§¹żĀĖ·ÖĄė³öĀČ»Æ¼Ųŗó£¬ĻņĀĖŅŗÖŠĶØŹŹĮæĀČĘųŃõ»ÆI££¬ÖʵĆø»µāČÜŅŗ”£ŹµŃéŹŅÄ£ÄāŃõ»Æ¹ż³ĢµÄŹµŃé×°ÖĆČēĶ¼ĖłŹ¾”£
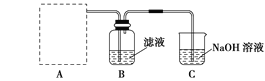
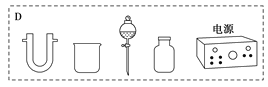
×°ÖĆÖŠA²æ·ÖÓĆÓŚÖĘČ”ĀČĘų£¬ŹµŃéŹŅÖĘČ”ĀČĘųĶس£ÓŠĮ½ÖÖ·½°ø£ŗŅ»ŹĒŌŚĒæĖįŠŌĢõ¼žĻĀÓĆŃõ»Æ¼ĮŃõ»ÆCl££»¶žŹĒµē½ā·Ø”£ĻŽÓĆĶ¼DÖŠµÄŅĒĘ÷(Ö§³ÅŅĒĘ÷”¢µ¼¹Ü”¢µ¼Ļß”¢ŹÆÄ«°ōŗĶĻšĘ¤Čū³żĶā)£¬ÄÜŹµĻֵķ“Ó¦ŹĒ___(Ń”Ģī±ąŗÅ)”£
a£®2NaCl(s)£«MnO2£«2H2SO4(ÅØ)![]() MnSO4£«Cl2”ü£«Na2SO4£«2H2O
MnSO4£«Cl2”ü£«Na2SO4£«2H2O
b£®2KMnO4£«16HCl(ÅØ)”ś2MnCl2£«2KCl£«5Cl2”ü£«8H2O
c£®2NaCl£«2H2O![]() 2NaOH£«Cl2”ü£«H2”ü
2NaOH£«Cl2”ü£«H2”ü
d£®4HCl(ÅØ)£«MnO2![]() MnCl2£«Cl2”ü£«2H2O
MnCl2£«Cl2”ü£«2H2O
¹ćæŚĘæBÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ____”£×°ÖĆCÖŠNaOHµÄ×÷ÓĆŹĒ___”£
(3)²½ÖčČż£ŗČ”100 mL BÖŠø»µāČÜŅŗ£¬°“ČēĻĀĮ÷³Ģ·ÖĄėµāµ„ÖŹ”£
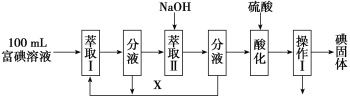
ŻĶČ”¢ņŗĶĖį»Æ¹ż³Ģ·¢ÉśµÄĄė×Ó·“Ó¦·½³ĢŹ½·Ö±šŹĒ£ŗ
3I2+6OH-=5I-+IO3-+3H2O£»____£»
ŻĶČ”¼ĮXӦєŌń____(Ń”Ģī±ąŗÅ)”£
a£®100mL±½ b£®10mLŅŅ“¼ c£®10 mLCCl4 d£®10mL¼ŗĻ©
ŹµŃéŹŅ½ųŠŠŻĶČ”²Ł×÷µÄŅĒĘ÷ŹĒ_____”£²Ł×÷¢ńµÄĆū³ĘŹĒ___”£
(4)·ÖĄė³öµÄKClѳʷ֊³£ŗ¬ÓŠÉŁĮæNaClŗĶK2CO3µČĪļÖŹ£¬Éč¼ĘŹµŃéÓĆ³Įµķ·Ø²ā¶ØĀČ»Æ¼Ųѳʷ֊K2CO3µÄÖŹĮæ·ÖŹż£ŗ¢ŁŅŖÓƵ½µÄ»ÆѧŹŌ¼ĮŹĒ___(ĢīŠ“»ÆѧŹ½)£»¢ŚŅŖ²ā¶ØµÄĪļĄķĮæŹĒ_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĢžAµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ84£®»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)ČōĢžAĪŖĮ“Ģž£¬·Ö×ÓÖŠĖłÓŠµÄĢ¼Ō×ÓŌŚĶ¬Ņ»Ę½ĆęÉĻ£¬øĆ·Ö×ÓµÄŅ»ĀČČ”“śĪļÖ»ÓŠŅ»ÖÖ”£
¢Ł AµÄ½į¹¹¼ņŹ½ĪŖ___________________________Ćū³ĘĪŖ____________________________
¢Ś Į“ĢžAÓėBr2µÄCCl4ČÜŅŗ·“Ӧɜ³ÉB£¬Š“³öÓÉAÉś³ÉBµÄ»Æѧ·½³ĢŹ½£ŗ______________
¢Ū ÓėA»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬ĒŅÖ÷Į“Ģ¼Ō×ÓøöŹżÓėAĻąĶ¬µÄĮ“ĢžÓŠ_____ÖÖ(²»°üĄØA)
(2)ČōA²»ÄÜŹ¹äåĖ®ĶŹÉ«£¬ĒŅ·Ö×ÓÖŠÖ»ÓŠŅ»ÖÖ»Æѧ»·¾³µÄĒāŌ×Ó£¬ŌņAµÄ½į¹¹¼ņŹ½ĪŖ_______________
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æNa2SO3ČÜŅŗ×÷ĪŖĪüŹÕŅŗĪüŹÕSO2Ź±£¬ĪüŹÕŅŗpHĖęn(SO32-)”Ćn(HSO3-)±ä»ÆĶ¼ĻńČēĶ¼£ŗ
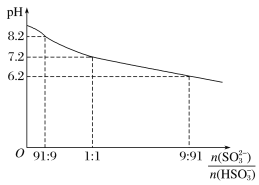
ŌņŅŌĻĀĄė×ÓÅØ¶Č¹ŲĻµµÄÅŠ¶ĻÕżČ·µÄŹĒ
A. NaHSO3ČÜŅŗÖŠc(H£«)£¼c(OH£)
B. Na2SO3ČÜŅŗÖŠc(Na£«)£¾c(SO32-)£¾c(HSO3-)£¾c(OH£)£¾c(H£«)
C. µ±ĪüŹÕČÜŅŗ³ŹÖŠŠŌŹ±£¬c(Na£«)£¾c(SO32-)£¾c(HSO3-)£¾c(OH£)£½c(H£«)
D. µ±ĪüŹÕČÜŅŗ³ŹÖŠŠŌŹ±£¬c(Na£«)£¾c(HSO3-)£«c(SO32-)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŅĻ©ĆŃŹĒŅ»ÖÖĀé×ķ¼Į£¬ĘäŗĻ³ÉĀ·ĻßČēĶ¼£¬ÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
![]()
A. XæÉÄÜŹĒBr2B. XæÉÄÜĪŖHO©Cl
C. ŅŅĻ©ĆŃŅ×ČÜÓŚĖ®D. ¢Ł¢Ś¢Ū·“Ó¦ĄąŠĶŅĄ“ĪĪŖČ”“ś”¢Č”“śŗĶĻūČ„
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖ£ŗA(g)£«2B(g) ![]() 2C(g)””¦¤H£½£Q kJ”¤mol£1(Q>0)£¬ŌŚŗćČŻµÄĆܱÕČŻĘ÷ÖŠ³äČė1 mol AŗĶ2 mol B£¬Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ(””””)
2C(g)””¦¤H£½£Q kJ”¤mol£1(Q>0)£¬ŌŚŗćČŻµÄĆܱÕČŻĘ÷ÖŠ³äČė1 mol AŗĶ2 mol B£¬Ņ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ(””””)
A. Ę½ŗāĒ°£¬Ėę×Å·“Ó¦µÄ½ųŠŠ£¬ČŻĘ÷ÄŚĘųĢåĆܶČÖš½„¼õŠ”
B. Ę½ŗāŹ±£¬øĆ·“Ó¦·Å³öµÄČČĮæĪŖQ kJ
C. Ę½ŗāŗó£¬ŌŁĻņČŻĘ÷ÖŠĶØČė1 molŗ¤Ęų£¬AµÄ×Ŗ»ÆĀŹŌö“ó
D. Ę½ŗāŗó£¬ĖõŠ”ČŻĘ÷ČŻ»ż£¬AµÄÅضČŌö“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ·“Ó¦ÖŠĖ®Ö»±ķĻÖ»¹ŌŠŌµÄŹĒ
A. 3NO2£«H2O=2HNO3£«NO
B. 2H2O ![]() 2H2”ü£«O2”ü
2H2”ü£«O2”ü
C. 2F2£«2H2O=4HF£«O2
D. 2Na£«2H2O=2NaOH£«H2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©0.4 molijĘųĢåµÄĢå»żĪŖ9.8 L£¬ŌņøĆĘųĢåµÄĦ¶ūĢå»żĪŖ____________”£
£Ø2£©ÓŠ±ź×¼×“æöĻĀµÄĖÄÖÖĘųĢå:¢Ł6.72 L CH4£¬¢Ś3.01”Į1023øöH2·Ö×Ó£¬¢Ū3.4 g H2S£¬¢Ü0.2 mol NH3£¬ŌņĘäĢå»ż°““ӓ󵽊”µÄĖ³ŠņĪŖ:_________________£ØĢīŠņŗÅ£©”£
£Ø3£©±ź×¼×“æöĻĀ£¬²āµĆ1.92æĖijĘųĢåµÄĢå»żĪŖ672 mL£¬Ōņ“ĖĘųĢåµÄĻą¶Ō·Ö×ÓÖŹĮæĪŖ__________
£Ø4£©ŹµŃéŹŅÓĆNa2CO3”¤10H2O¾§ĢåÅäÖĘ0.5mol/LµÄNa2CO3ČÜŅŗ970mL£¬Ó¦³ĘČ”Na2CO3”¤10H2OµÄÖŹĮæŹĒ___________”£
£Ø5£©Ä³Ń§ÉśÓūÓĆ12mol”¤L£1ÅØŃĪĖįŗĶÕōĮóĖ®ÅäÖĘ500 mL 0.3 mol”¤L£1µÄĻ”ŃĪĖį”£
¢ŁøĆѧɜŠčŅŖĮæČ”________mLÉĻŹöÅØŃĪĖį½ųŠŠÅäÖĘ”£
¢ŚĻĀĮŠŹµŃé²Ł×÷»įµ¼ÖĀĖłÅäÖʵÄĻ”ŃĪĖįµÄĪļÖŹµÄĮæÅضČĘ«Š”µÄŹĒ__________£ØĢīŠņŗÅ£©”£
a.ÓĆĮæĶ²ĮæČ”ÅØŃĪĖįŹ±ø©ŹÓ¹Ū²ģ°¼ŅŗĆę
b.½«ĮæČ”ÅØŃĪĖįµÄĮæĶ²½ųŠŠĻ“µÓ£¬²¢½«Ļ“µÓŅŗ×ŖŅʵ½ČŻĮæĘæÖŠ
c.Ļ”ŹĶÅØŃĪĖįŹ±£¬Ī“ĄäČ“µ½ŹŅĪĀ¼“×ŖŅʵ½ČŻĮæĘæÖŠ
d. ¶ØČŻŗó¾Õńµ“”¢Ņ”ŌČ”¢¾²ÖĆ£¬·¢ĻÖŅŗĆęĻĀ½µ£¬ŌŁ¼ÓŹŹĮæµÄÕōĮóĖ®
e.ČŻĮæĘæĻ“µÓøɾ»ŗóĪ“øÉŌļ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com