
亚氯酸钠(NaClO2)是一种高效氧化剂和漂白剂,主要用于棉纺、纸浆漂白和鱼药的制造。制备亚氯酸钠的工艺流程如下:

(1)要加快步骤①的反应速率,可采取的措施为 。(写一种即可)
(2)步骤①的离子方程式为 ,每生成标准状况下22.4L的ClO2,转移电子数为 。
(3)步骤②中H2O2的作用是 ;从“反应混合液”到“产品”的过程中先需蒸发溶剂,写出蒸发所需的硅酸盐仪器的名称 。
(4)NaClO2产品中通常混有少量NaCl。取样品wg,测得Na的物质的量为nmol,则该样品中NaClO2的物质的量为______mol。
科目:高中化学 来源:2015-2016学年四川成都七中高一下甲烷课后作业化学试卷(解析版) 题型:选择题
下列物质之间的相互关系错误的是( )
A.CH3CH2OH和CH3OCH3互为同分异构体
B.干冰和冰为同一种物质
C.CH3CH3和CH3CH2CH3互为同系物
D.O2和O3互为同素异形体
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三最后一次模拟理综化学试卷(解析版) 题型:推断题
【化学一有机化学基础】已知:R-CH=CH-O-R′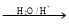 R-CH2CHO + R′OH(烃基烯基醚)烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3∶4 。与A相关的反应如下:
R-CH2CHO + R′OH(烃基烯基醚)烃基烯基醚A的相对分子质量(Mr)为176,分子中碳氢原子数目比为3∶4 。与A相关的反应如下:
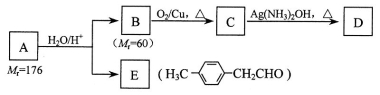
请回答下列问题:
(1) A的结构简式为_____________________、含有的官能团为 (写名称);
(2) E的名称是___________________;
(3) 写出C → D反应的化学方程式:_______________________________________。
(4) 同时满足下列条件的E的同分异构体有 种:K^S*5U.C#O
①属于芳香醛;② 苯环上有两种不同环境的氢原子。
其中核磁共振氢谱为5组峰的为其峰面积之比为3∶2∶2∶2∶1______________(写结构简式)
(5)由E转化为对甲基苯乙炔(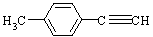 )的一条路线如下:
)的一条路线如下:
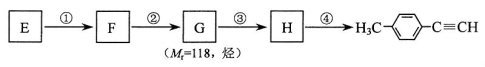
ⅰ. 写出G的结构简式:____________________________________。K^S*5U.C#O
ⅱ. 写出①~④步反应所加试剂、反应条件和反应类型:
序号 | 所加试剂及反应条件 | 反应类型 |
① | ||
② | ||
③ | ||
④ |
查看答案和解析>>
科目:高中化学 来源:2016届福建厦门外国语学校高三5月月考理综化学试卷(解析版) 题型:实验题
TiO2和TiCl4都是钛的重要化合物,某化学兴趣小组在实验室对两者的制备及性质进行探究。
Ⅰ.制备TiCl4
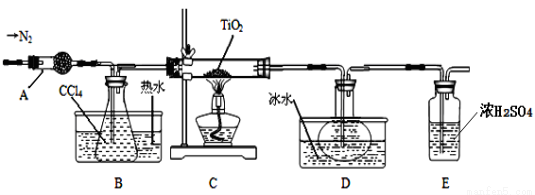
实验室利用反应TiO2 (s)+CCl4(g) TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,装置图和有关信息如下:
TiCl4(g)+CO2(g),在无水无氧条件下制备TiCl4,装置图和有关信息如下:
物质 | 熔点/℃ | 沸点/℃ | 其他 |
CCl4 | —23 | 76 | 与TiCl4互溶 |
TiCl4 | —25 | 136 | 遇潮湿空气产生白雾 |
请回答下列问题:
(1)仪器A的名称是 。
(2)实验开始前后的操作包括:①检查装置气密性,②组装仪器,③通N2一段时间,④加装药品,⑤点燃
酒精灯⑥停止通N2⑦停止加热。正确的操作顺序是__________________________。实验结束后欲分离D中的液态混合物,所采用操作的名称是 。
(3)装置E能否 (填“能”或“不能”)换成装置A,理由是 。
(4)TiCl4是制取航天航空工业材料——钛合金的重要原料。某钛合金的元素还有Al和Si等,已知在常温下,钛是一种耐强酸强碱的金属,请设计实验检验其中的Si元素。 。
Ⅱ.制备TiO2及测定TiO2的质量分数:
在TiCl4中加水、加热,水解得到沉淀TiO2·xH2O,经过滤、水洗,再烘干、焙烧除去水分得到粉体TiO2。
(5)写出生成TiO2·xH2O的化学方程式 。
(6)检验沉淀是否洗涤干净的方法是___________________________________________。
(7) 一定条件下,将TiO2溶解并还原为Ti3+,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。滴定分析时,称取上述TiO2试样0.2g,消耗0.1 mol·L-1 NH4Fe(SO4)2标准溶液20mL 。
。
①配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的目的是: 。
②该滴定操作所用到的指示剂是 。
③则TiO2质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2016届福建厦门外国语学校高三5月月考理综化学试卷(解析版) 题型:选择题
晚唐诗人李商隐的《无题·相见时难别亦难》中写到“春蚕到死丝方尽,蜡炬成灰泪始干”,下列说法正确的是
A.蚕丝属于纤维素
B.蜡烛的主要成分是石蜡,属于混合物
C.“泪”是指石蜡燃烧生成的水
D.蚕丝和石蜡完全燃烧所得产物相同
查看答案和解析>>
科目:高中化学 来源:2016届安徽师大附中高三最后一卷理综化学试卷(解析版) 题型:选择题
下列有关说法正确的是
A.2,2-二甲基丁烷与2,4-二甲基戊烷的一氯代物种类相同
B.乙烷、苯、葡萄糖溶液均不能使酸性高锰酸钾溶液褪色
C.苯的密度比水小,但由苯反应制得的溴苯、硝基苯、环己烷的密度都比水大
D.乙酸乙酯在碱性条件下的水解反应称为皂化反应
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三热身考试理综化学试卷(解析版) 题型:填空题
(16分)汽车尾气中的主要污染物是NO和CO。为减轻大气污染,人们提出通过以下反应来处理汽车尾气:
(1)2NO(g)+2CO(g)?2CO2(g)+N2(g)△H=﹣746.5KJ/mol (条件为使用催化剂)
已知:2C (s)+O2(g)?2CO(g)△H=﹣221.0KJ/mol
C (s)+O2(g)?CO2(g)△H=﹣393.5KJ/mol
则N2(g)+O2(g)=2NO(g)△H= kJ•mol﹣1。
(2)T℃下,在一容积不变的密闭容器中,通入一定量的NO和CO,用气体传感器测得不同时间NO和CO的浓度如下表
时间/s | 0 | 1 | 2 | 3 | 4 | 5 | |||||||
C(NO)10﹣4 mol/L | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 | |||||||
C(CO)10﹣3 mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 | |||||||
则C2合理的数值为 (填字母标号)。
A.4.20 B.4.00 C.2.95 D.2.80
(3)将不同物质的量的H2O(g)和CO(g)分别通入体积为2L的恒容密闭容器中,进行反应:H2O(g)+CO(g)?CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | CO | H2 | |||
i | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
ii | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
iii | 900 | a | b | c | d | t |
若a=2,b=1,则c= ,达平衡时实验组ii中H2O(g)和实验组iii中CO的转化率的关系为αii(H2O) αiii(CO)(填“<”、“>”或“=”)。
(4)二甲醚是清洁能源,用CO在催化剂存在下制备二甲醚的反应原理为:2CO(g)+4H2(g)?CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比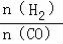 的变化曲线如图1所示。
的变化曲线如图1所示。
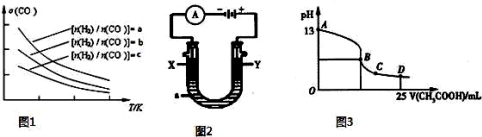
①a、b、c按从大到小的顺序排序为 。
②根据图象可以判断该反应为放热反应,理由是 。
(5)CO分析仪的传感器可测定汽车尾气是否符合排放标准,该分析仪的工作原理类似于燃料电池,其中电解质是氧化钇(Y2O3)和氧化锆(ZrO2)晶体,能传导O2﹣。
①则负极的电极反应式为 。
②以上述电池为电源,通过导线连接成图2.若X、Y为石墨,a为2L 0.1mol/L KCl溶液电解一段时间后,取25mL 上述电解后的溶液,滴加0.4mol/L醋酸得到图3曲线(不考虑能量损失和气体溶于水,溶液体积变化忽略不计).根据图二计算,上述电解过程中 消耗一氧化碳的质量为 g。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高二下期中化学试卷(解析版) 题型:选择题
下列说法中正确的是
A.某反应在低温条件下能自发进行,那么该反应在高温条件下也一定能自发进行
B.某反应在高温条件下不能自发进行,那么该反应在低温条件下也一定不能自发进行
C.反应方向是由焓变和熵变共同决定的,与反应温度无关
D.温度有可能对反应的方向起决定性作用
查看答案和解析>>
科目:高中化学 来源:2015-2016学年天津市高一6月学业调研化学试卷(解析版) 题型:选择题
在强酸性或强碱性溶液中都能大量共存的一组离子是
A.Ba2+、Fe3+、Br一、NO3—
B.Na+、Ca2+、HCO3—、NO3—
C.A13+、NH4+、SO42—、Na+
D.Na+、K+、NO3—、SO42—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com