
【题目】光气(COCl2)又称碳酰氯,下列关于光气的叙述中正确的是
A.COCl2中含有2个σ键和1个π键
B.COCl2中C原子杂化轨道类型为sp2
C.COCl2为含极性键和非极性键的极性分子
D.COCl2分子的空间构型为三角锥形
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】下列有关乙烯和苯分子中的化学键描述正确的是( )
A.苯分子中每个碳原子的![]() 杂化轨道中的其中一个形成大
杂化轨道中的其中一个形成大![]() 键
键
B.乙烯分子中![]() 键是
键是![]() 杂化轨道形成的
杂化轨道形成的![]() 键
键![]() 键是未参加杂化的
键是未参加杂化的![]() 轨道形成的
轨道形成的![]() 键
键
C.苯分子中碳碳键是![]() 杂化轨道形成的
杂化轨道形成的![]() 键,
键,![]() 键是未参加杂化的
键是未参加杂化的![]() 轨道形成的
轨道形成的![]() 键
键
D.乙烯和苯分子中每个碳原子都以![]() 杂化轨道形成
杂化轨道形成![]() 键,未杂化的
键,未杂化的![]() 轨道形成
轨道形成![]() 键
键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是极易溶于水的气体,常温常压下,1体积水大约能溶解700体积的氨气。
(1)实验室可在浓氨水中加入固体NaOH快速制取氨气,请用化学平衡移动原理简述原因___。
(2)甲、乙两瓶氨水的浓度分别为1mol·L-1和0.1mol·L-1,则甲、乙两瓶氨水中c(OH-)之比___(填“>”、“<”或“=”)10。
(3)向10mL0.1mol/L的氨水中逐滴加入20mL0.1mol/L的醋酸,溶液导电性的变化是___。写出二者反应的离子方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某科研小组模拟“人工树叶”电化学装置如图所示,甲装置能将H2O和CO2转化为C6H12O6和O2,X、Y是特殊催化剂型电极,乙装置为甲醇—空气燃料电池。下列说法不正确的是

A.b口通入空气,c口通入甲醇
B.甲装置中H+向X极移动,乙装置中H+向M极移动
C.理论上,每生成22.4LO2(标况下),必有4mol电子由N极移向X极
D.阳极上的电极反应式为6CO2 + 24H+ + 24e- = C6H12O6 + 6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分前36号元素的性质或原子结构信息如下表:
元素编号 | 元素的性质或原子结构 |
R | 基态原子的最外层有3个未成对电子,次外层有2个电子 |
S | 单质能与水剧烈反应,所得溶液a弱酸性 |
T | 基态原子3d轨道上有1个电子 |
X |
|
(1)R元素的第一电离能要大于其同周期相邻的元素,原因是______。
(2)S元素的常见化合价为_______,原因是_______。
(3)T元素的原子N电子层上的电子数为____________。
(4)X的轨道表示式违背了____________。用X单质、碱金属盐等可以制作焰火。燃放时,焰火发出五颜六色的光,请用原子结构的知识解释发光的原因:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料。三氯化硼(BCl3)可用于制取乙硼烷(B2H6),也可作有机合成的催化剂。
查阅资料 ①BCl3的沸点为12.5 ℃,熔点为-107.3 ℃;②2B+6HCl△2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应。
设计实验 某同学设计如图所示装置制备三氯化硼:
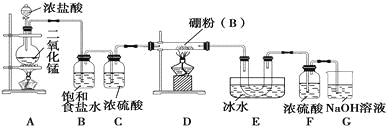
请回答下列问题:
(1)常温下,高锰酸钾固体粉末与浓盐酸发生的反应可替代A装置中的反应,而且不需要加热,两个反应的产物中锰的价态相同。写出高锰酸钾固体粉末与浓盐酸反应的离子方程式:_________________。
(2)E装置的作用是___________。如果拆去B装置,可能的后果是_________________。
(3)实验中可以用一个盛装___(填试剂名称)的干燥管代替F和G装置,使实验更简便。
(4)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式:____________;实验室保存三氯化硼的注意事项是_______。
(5)为了顺利完成实验,正确的操作是_______(填序号).
①先点燃A处酒精灯,后点燃D处酒精灯
②先点燃D处酒精灯,后点燃A处酒精灯
③同时点燃A、D处酒精灯
(6)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓_______(填化学式)溶液,若有气泡产生,则样品中含有硼粉;若无气泡产生,则样品中无硼粉。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某锂离子电池正极材料有钴酸锂(LiCoO2)、石墨和铝箔等,该电池充电时负极(阴极)反应为6C+xLi++xe- = LixC6,锂电池充放电过程中发生LiCoO2与Li1-xCoO2之间的转化。现利用以下工艺回收正极材料中的某些金属资源。
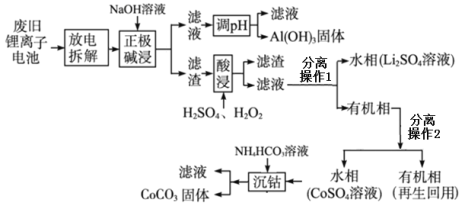
回答下列问题:
(1)放电时电池总反应方程式_______________;该工艺首先将废旧电池“放电处理”的目的除安全外还有_______________。
(2)写出“正极碱浸”过程中发生反应的离子方程式_______________。
(3) 分离操作1是_______________;“酸浸”步骤发生的氧化还原反应化学方程式是_______________。
(4)“酸浸”时若用盐酸代替H2SO4和H2O2的混合液,缺点是_______________。
(5)“沉钴”过程中的实验现象有_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A、B、C三种分子所含原子的数目依次为1、3、6,且分子中均含有18个电子,B、C是由两种元素组成的,且分子中两种元素原子的个数比均为1:2。请回答下列问题。
(1)A的分子式是__________,写出A原子的价电子排布式:__________
(2)B分子的中心原子的杂化类型是__________,分子的空间构型是__________,该分子属于__________(填“极性”或“非极性”)分子。
(3)C的化学式是__________,分子中含有的化学键类型是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用键线式表示,如:
结构简式 |
|
|
|
键线式 |
|
|
|
(1)![]() 的分子式为___________。
的分子式为___________。
(2)已知三个乙炔分子反应生成苯,试写出三个丙炔分子反应生成的芳香烃分子的键线式:__________(填一种即可)。
(3)由![]() 以及必要的无机试剂可合成
以及必要的无机试剂可合成 ,写出第一步合成反应的化学方程式:________。
,写出第一步合成反应的化学方程式:________。
(4)A为![]() 的一种同分异构体,A的一氯代物有三种,且A与
的一种同分异构体,A的一氯代物有三种,且A与![]() 按物质的量之比为
按物质的量之比为![]() 加成得到的产物只有一种(不考虑顺反、立体异构),则A可能的结构简式有_____________。
加成得到的产物只有一种(不考虑顺反、立体异构),则A可能的结构简式有_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com