
【题目】一种气态烷烃和一种气态烯烃的混合物9g,其密度是相同条件下氢气密度的11.25倍,当混合气体通过足量溴水时,溴水增重4.2g,则这两种气态烃是( )
A.甲烷和乙烯
B.乙烷和乙烯
C.甲烷和丙烯
D.甲烷和丁烯
【答案】C
【解析】解:混合气体的密度是相同状况下H2密度的11.25倍可以确定有机物的平均摩尔质量22.5g/mol,故混合气体中一定有甲烷,混合气体的总的物质的量为 ![]() =0.4mol;该混合气通过Br2水时,Br2水增重4.2g,4.2g为烯烃的质量,所以甲烷的质量为9g﹣4.2g=4.8g,甲烷的物质的量为:
=0.4mol;该混合气通过Br2水时,Br2水增重4.2g,4.2g为烯烃的质量,所以甲烷的质量为9g﹣4.2g=4.8g,甲烷的物质的量为: ![]() =0.3mol,则烯烃的物质的量为0.4mol﹣0.3mol=0.1mol,
=0.3mol,则烯烃的物质的量为0.4mol﹣0.3mol=0.1mol,
所以M(烯烃)= ![]() =42gmol﹣1 ,
=42gmol﹣1 ,
设烯烃的组成为CnH2n , 则14n=42,所以n=3,为丙烯,
所以混合物为甲烷、丙烯,
故选C.
根据混合气体的密度是相同状况下H2密度的11.25倍可以确定有机物的平均摩尔质量22.5g/mol,故混合气体中一定有甲烷,混合气体的总的物质的量为: ![]() =0.4mol;该混合气通过Br2水时,Br2水增重4.2g,4.2g为烯烃的质量,所以甲烷的质量为4.8g,物质的量为0.3mol,故烯烃的物质的量为0.1mol,结合烯烃的质量和物质的量来确定烯烃的摩尔质量,再根据烯烃组成通式确定烯烃.
=0.4mol;该混合气通过Br2水时,Br2水增重4.2g,4.2g为烯烃的质量,所以甲烷的质量为4.8g,物质的量为0.3mol,故烯烃的物质的量为0.1mol,结合烯烃的质量和物质的量来确定烯烃的摩尔质量,再根据烯烃组成通式确定烯烃.


科目:高中化学 来源: 题型:
【题目】在下列溶液中,各组离子一定能够大量共存的是( )
A.能使广泛pH试纸显蓝色的溶液:K+、Ba2+、Cl﹣、Br﹣
B.常温下 ![]() =12的溶液:Fe2+、Mg2+、NO3﹣、Cl﹣
=12的溶液:Fe2+、Mg2+、NO3﹣、Cl﹣
C.含有大量Al3+的溶液中:Na+、Cl﹣、AlO2﹣、OH﹣
D.能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42﹣、S2﹣、SO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学研究性学习小组设计实验探究铜的常见化学性质,过程设计如下:提出猜想
问题1:在周期表中,铜与铝的位置很接近,铜不如铝活泼,氢氧化铝具有两性,氢氧化铜也有两性吗?
问题2:铁和铜都有变价,一般情况下,正二价铁的稳定性小于正三价的铁,正一价铜的稳定性也小于正二价的铜吗?
问题3:氧化铜有氧化性,能被H2、CO还原,它也能被氮的某种气态氢化物还原吗?
实验探究
(1)I.解决问题1a.需用到的药品除1molL﹣1CuSO4溶液、稀硫酸外还需(填试剂的化学式)溶液.
b.用胆矾晶体配制1molL﹣1CuSO4溶液250mL,选用的仪器除烧杯、托盘天平、药匙、
玻璃棒、胶头滴管外,还有(填仪器名称).
c.为达到实验目的,请你补全实验内容和步骤:
①用CuSO4溶液制备Cu(OH)2;
② .
(2)Ⅱ.解决问题2取一定量I中制备获得的氢氧化铜固体于坩埚中灼烧,当温度达到80~100℃得到黑色固体粉末;继续加热至1000℃以上,黑色粉末全部变成红色粉末氧化亚铜;取适量红色氧化亚铜粉末于洁净试管中,加入过量的稀硫酸(或盐酸),得到蓝色溶液,同时观察到试管底部还有红色固体存在.根据以上实验现象回答问题.
a.写出氧化亚铜与稀硫酸(或盐酸)反应的离子方程式: .
b.从实验Ⅱ可得出的结论是在高温下正一价铜比正二价铜(填稳定或不稳定),
溶液中正一价铜比正二价铜(填稳定或不稳定).
(3)Ⅲ.解决问题3设计如下装置(夹持装置未画出):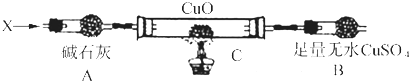
当氮的某种气态氢化物(X)缓缓通过灼热的氧化铜时,观察到氧化铜由黑色变成了红色,无水硫酸铜变成蓝色,生成物中还有一种无污染的单质气体Y;将X通人灼热的CuO燃烧管完全反应后,消耗0.01mol X,测得B装置增重0.36g,并收集到0.28g气体Y.
a.仪器A的名称是 .
b.X的化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关煤和石油的加工方法的叙述中错误的是( )
A.通过煤的直接或间接液化可以获得各种芳香烃
B.通过石油的催化重整等工艺可获取芳香烃
C.石油的裂化的目的主要是为了提高轻质油的产量
D.石油的裂解的目的主要是为了获取不饱和烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向10.0mL 0.10molL﹣1氨水中滴入0.10molL﹣1的盐酸,溶液的pH与所加盐酸的体积关系如图所示(假设无气体逸出),下列有关叙述正确的是( ) 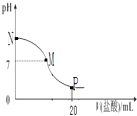
A.M﹣N间一定存在c(Cl﹣)>c(NH4+)>c(OH﹣)>c(H+)
B.M点对应的盐酸体积为10.0mL
C.pH=7溶液中有c(NH4+)=c(Cl﹣)=c(H+)=c(OH﹣)
D.P点处的溶液中存在:2c(NH4+)+2c(NH3H2O)=c(Cl﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚.其反应原理如下:电池:Pb(s)+PbO2(s)+2H2SO4(aq)=2PbSO4(s)+2H2O(l);电解池:2Al+3H2O ![]() Al2O3+3H2↑,电解过程中,以下判断正确的是( )
Al2O3+3H2↑,电解过程中,以下判断正确的是( )
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3molPb | 生成2molAl2O3 |
C | 正极:PbO2+4H++2e﹣=Pb2++2H2O | 阳极:2Al+3H2O﹣6e﹣=Al2O3+6H+ |
D |
|
|
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学反应速率及化学平衡,下列说法中正确的个数是
①恒温时,增大压强,化学反应速率一定加快
②其他条件不变,温度越高,活化分子百分数增加,活化分子浓度也增加,反应速率加快
③使用催化剂可改变反应速率,从而改变该反应过程中吸收或放出的热量
④3mol·L-1·s-1的反应速率一定比1mol·L-1·s-1的反应速率大
⑤正反应速率越大,反应朝正反应方向进行的程度越大
⑥增加反应物的浓度,活化分子浓度增加,反应速率加快
⑦平衡向正反应方向移动,反应物的转化率都增大
⑧若在一定条件下,平衡向正反应方向移动,则正反应速率变大
⑨化学平衡常数越小,说明正反应进行程度越小,即该反应进行的就越不完全,转化率就 越小
⑩温度越高,化学平衡常数就越大
A. 3个 B. 4个 C. 5个 D. 6个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com