
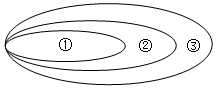
| A. | ①CO、②酸性氧化物、③氧化物 | B. | ①Na2CO3、②钠盐、③碳酸盐 | ||
| C. | ①胶体、②分散系、③混合物 | D. | ①单质、②化合物、③纯净物 |
分析 A、能和碱反应生成盐和水的氧化物为酸性氧化物;
B、碳酸钠的阳离子是钠离子,阴离子是碳酸根离子;
C、将一种物质分散到另一种物质中所得到的体系为分散系;
D、只由一种物质构成的是纯净物.
解答 解:A、能和碱反应生成盐和水的氧化物为酸性氧化物,CO既不是酸性氧化物也不是碱性氧化物,即①不属于②,故A错误;
B、碳酸钠的阳离子是钠离子,阴离子是碳酸根离子,故碳酸钠为钠盐,也为碳酸盐,即①既属于②也属于③,但②不属于③,故B错误;
C、将一种物质分散到另一种物质中所得到的体系为分散系,分为溶液、胶体和浊液,故胶体属于分散系,而分散系属于混合物,故C正确;
D、只由一种物质构成的是纯净物,分为单质和化合物,①②均属于③,但①和②是并列关系,故D错误.
故选C.
点评 本题考查了常见概念之间的从属关系,掌握概念是解题关键所在,应注意的是氧化物分为酸性氧化物、碱性氧化物、两性氧化物和不成盐氧化物等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤⑧ | B. | ⑦④ | C. | ①③ | D. | ⑤⑥⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加生石灰,过滤 | B. | 加适量的AgNO3溶液 | ||
| C. | 加过量的Na2CO3溶液 | D. | 加CaCO3粉末,过滤 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铁溶液、高锰酸钾酸性溶液 | B. | 碳酸钠溶液、溴水 | ||
| C. | 新制的银氨溶液溶液、溴水 | D. | 新制氢氧化铜悬浊液、氯化铁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 已知某市售“84消毒液”瓶体部分标签如下图所示,该“84 消毒液”通常稀释100 倍(体积之比)后使用. 请回答下列问题:
已知某市售“84消毒液”瓶体部分标签如下图所示,该“84 消毒液”通常稀释100 倍(体积之比)后使用. 请回答下列问题:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com