
| 6.72L |
| 22.4L/mol |
| 3.01��1023 |
| 6.02��1023/mol |
| 13.6g |
| 34g/mol |
| V |
| Vm |
| m |
| M |
| 2m |
| M |
| ||
| V��10-3L |
| 2000m |
| MV |
| mg |
| ��Vg |
| 100m |
| ��V |
| 2000m |
| MV |
| 100m |
| ��V |


 ��ĩ100�ִ��غ�������ϵ�д�
��ĩ100�ִ��غ�������ϵ�д� Сѧ�������Ծ�ϵ�д�
Сѧ�������Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ij��ѧ��Ӧ2A��g��?B��g������Ӧ�����������仯��ͼ��ʾ��ͼ��E1 ��ʾ����Ӧ�Ļ�ܣ�E2 ��ʾ�淴Ӧ�Ļ�ܣ��������й�������ȷ���ǣ�������
ij��ѧ��Ӧ2A��g��?B��g������Ӧ�����������仯��ͼ��ʾ��ͼ��E1 ��ʾ����Ӧ�Ļ�ܣ�E2 ��ʾ�淴Ӧ�Ļ�ܣ��������й�������ȷ���ǣ�������| A���÷�ӦΪ���ȷ�Ӧ |
| B���������ı�÷�Ӧ���ʱ� |
| C���������ܸı䷴Ӧ·�������ܽ��÷�Ӧ�Ļ�� |
| D��������B�ȷ�Ӧ��Ӧ��A���ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
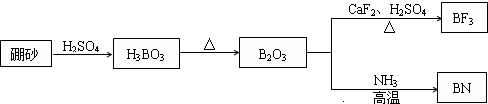
| Na2B2O7 | CaF2 | H3BO3 | NH3 | |
| A | ԭ�Ӿ��� | �������� | ԭ�Ӿ��� | ���Ӿ��� |
| B | ���Ӿ��� | ���Ӿ��� | ���Ӿ��� | ���Ӿ��� |
| C | ���Ӿ��� | ���Ӿ��� | ���Ӿ��� | ���Ӿ��� |
| D | ���Ӿ��� | ���Ӿ��� | ���Ӿ��� | ���Ӿ��� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
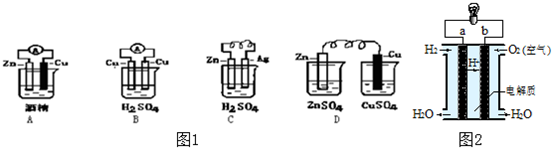
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ��װ�� | ʵ������ | ʵ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 1000��ʱ�������ƿ�������������Ӧ��Na2SO4��s��+4H2��g��?Na2S��s��+4H2O��g������ش��������⣺
1000��ʱ�������ƿ�������������Ӧ��Na2SO4��s��+4H2��g��?Na2S��s��+4H2O��g������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com