
【题目】某溶液中可能含有H+、NH4+、Fe3+、CO32-、SO42-、NO3-中的几种。
①若加入锌粒,产生无色无味的气体,且在空气中不变色;
②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加人NaO的物质的量之间的关系如下图所示。则下列说法正确的是

A.溶液中的阳离子只有H+、Mg2+、Al3 +
B.溶液中一定不含CO32-,可能含有SO42-和NO3-
C.溶液中n(NH4+)=0.2mol
D.n(H+):n(Al3+):n(Mg2+)=1:1:1
【答案】C
【解析】
试题分析:据图象特点可以知道:加入氢氧化钠先与氢离子反应再与镁铝离子反应生成氢氧化物沉淀,再与铵根反应得到一水合氨,氢氧化铝再与氢氧化铝反应生成偏铝酸钠,所以溶液中的阳离子一定含NH4+、H+、Mg2+、Al3+,故A错误;加锌产生无色无味气体说明锌与氢离子反应生成氢气溶液中有大量氢离子则没有碳酸根和硝酸根离子因为硝酸根氢离子与锌会反应生成刺激性的一氧化氮,故B错误;锂离子电池将化学能转化为电能,故B错误;根据图象特点可以知道:加入氢氧化钠先与氢离子反应再与镁铝离子反应生成氢氧化物沉淀再与铵根反应得到一水合氨再与氢氧化铝反应生成偏铝酸钠根据第二段是氢氧化钠与铵根反应得到一水合氨的阶段即NH4++OH-=NH3H2O消耗氢氧化钠的物质的量为0.7mol-0.5mol=0.2mol,所以溶液中n(NH4+)=0.2mol,故C正确;根据第一段是氢氧化钠中和氢离子的阶段所以氢离子的物质的量是0.1mol根据第四段是氢氧化铝和氢氧化钠反应的阶段即Al(OH)3~OH-~[Al(OH)4]-则消耗氢氧化钠的物质的量为:0.8mol-0.7mol=0.1mol,根据第二段是将铝离子和镁离子反应生成沉淀的阶段根据Al3+~3OH-~Al(OH)3、Mg2+~2OH-~Mg(OH)2 0.1mol氢氧化铝消耗氢氧化钠的物质的量是0.3mol,所以镁离子消耗氢氧化钠的物质的量是:0.5mol-0.1mol-0.3mol=0.1mol,所以镁离子的物质的量是0.05mol即n(H+):n(Al3+):n(Mg2+)=0.1:0.1:0.05=2:2:1,故D正确。


 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】若氨基酸的平均相对分子质量为a,一个由n条肽链组成的蛋白质分子共有m个氨基酸,则该蛋白质的相对分子质量为( )
A. am-18(m-n) B. am C. am-18(n-1) D. am-18n
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示3套实验装置,分别回答下列问题:

(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入碳棒的玻璃筒内滴入酚酞溶液,可观察到碳棒附近的溶液变红,该电极反应式为 。
(2)装置2中的石墨是 极(填“正”或“负”),该装置发生的总反应的离子方程式为 。
(3)装置3中甲烧杯盛放100 mL 0.2 mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5 mol/L的CuSO4溶液。反应一段时间后,停止通电。取出Cu电极,洗涤、干燥、称量、电极增重 0.64 g。
① 电源的M端为 极,甲烧杯中铁电极的电极反应式为 。
② 乙烧杯中电解总反应的离子方程式为 。
③ 甲、乙两烧杯中生成的气体在标况下共 mL。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 氯气能使湿润的有色布条褪色,所以氯气具有漂白性
B. 红热的铁丝在氯气中剧烈燃烧,反应生成氯化铁
C. 利用溴单质的氧化性可以把碘离子转化为碘单质
D. 实验室常用氢氧化钠溶液吸收多余的氯气以避免污染
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①能量越低的物质越稳定,②白磷转化成红磷放出热量。
据此,下列判 断或说法中正确的是
A. 在相同的条件下,红磷比白磷稳定
B. 在相同的条件下,白磷比红磷稳定
C. 红磷和白磷的结构相同
D. 红磷容易发生自燃而白磷则不会自燃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行以下实验,能得到相应实验结论的是( )
选项 | ① | ② | ③ | 实验结论 |
|
A | 稀硫酸 | 石灰石 | 澄清石灰水 | 制二氧化碳并吸收尾气 | |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
C | 稀盐酸 | Na2SO3 | H2S溶液 | SO2具有还原性 | |
D | 浓硝酸 | Na2CO3 | Na2SiO3 | 溶液酸性:硝酸>碳酸>硅酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知酸性K2Cr2O7溶液可与FeSO4反应生成Fe3+和Cr3+。现将硫酸酸化的K2Cr2O7溶液与FeSO4溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中Fe3+的物质的量随加入的KI的物质的量的变化关系如图所示,下列说法中不正确的是( )
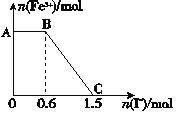
A.图中AB段的氧化剂为K2Cr2O7
B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2
C.开始加入的K2Cr2O7为0.15 mol
D.K2Cr2O7与FeSO4反应的物质的量之比为1∶6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I2在KI溶液中存在下列平衡:I2(aq)+I-(aq) ![]() I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
I3-(aq),某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法正确的是( )
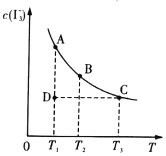
A.I2(aq)+I-(aq) ![]() I3-(aq)的△H>0
I3-(aq)的△H>0
B.若温度T1,T2的平衡常数分别为K1,K2,则K1>K2
C.反应进行到状态D时,一定有V正>V逆
D.状态A与状态B相比,状态A的c(I2)大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com