
分析 由2NaOH+H2SO4=Na2SO4+2H2O,可知n(NaOH)=2n(H2SO4),根据Na元素守恒计算n(Na),再根据m=nM计算Na的质量,进而计算NaCl的质量.
解答 解:由2NaOH+H2SO4=Na2SO4+2H2O,可知n(NaOH)=2n(H2SO4)=2×0.05L×2mol/L=0.2mol,根据Na元素守恒n(Na)=n(NaOH)=0.2mol,故m(Na)=0.2mol×23g/mol=4.6g,故m(NaCl)=6.2g-4.6g=1.6g,
答:混合物中Na的质量为4.6g,NaCl质量为1.6g.
点评 本题考查混合物计算、化学方程式计算,比较基础,注意对基础知识的理解掌握.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:选择题
| A. | $\frac{y-2x}{V}$ | B. | $\frac{2y-4x}{V}$ | C. | $\frac{2y-2x}{V}$ | D. | $\frac{y-x}{V}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正向移动 | B. | 逆向移动 | C. | 达到平衡 | D. | 不一定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验现象 | |
| 1.向打磨过的铝片中加入稀盐酸 | |
| 2.向打磨过的铝片中加入Na0H溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题
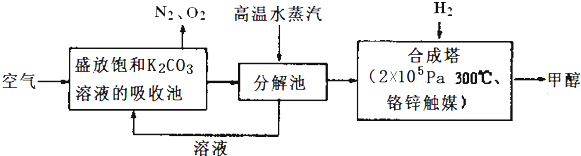
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c2=2c1 | B. | c2<2c1 | C. | c2>2c1 | D. | c1=2c2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com