
| 1.0×10-12 |
| 1.0×10-12 |
| 0.188g |
| 188g/mol |


科目:高中化学 来源: 题型:
| A、2mol FeSO4发生反应时,共有10 mol电子发生转移 |
| B、Na2FeO4既是氧化产物又是还原产物 |
| C、Na2FeO4处理水时,既能杀菌,又能在处理水时产生胶体净水 |
| D、Na2O2在上述反应中只作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属Fe与稀H2SO4反应:Fe+2H+═Fe3++H2↑ |
| B、Al(OH)3治疗胃酸过多:H++OH-═H2O |
| C、NaHCO3溶液与NaOH溶液混合:HCO3-+OH-═H2O+CO2↑ |
| D、Al与NaOH溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
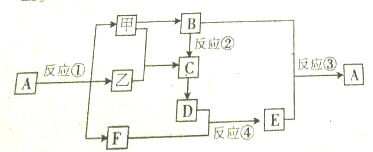
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
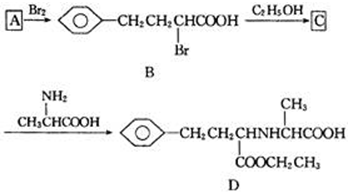
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图装置,C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
如图装置,C、D、E、F都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.查看答案和解析>>
科目:高中化学 来源: 题型:
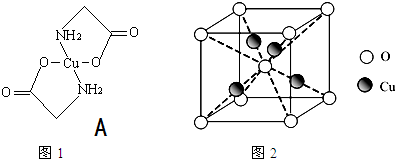
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com