
 .下列说法正确的是( )
.下列说法正确的是( )| A. | 化合物X在空气中能稳定存在 | |
| B. | 化合物X中所有碳原子可处于同一平面 | |
| C. | 化合物X、Y都可与溴水发生加成反应 | |
| D. | 1 mol化合物Y最多可以与4 mol H2反应 |
分析 A.X中含酚-OH;
B.苯环、羰基为平面结构,且二者直接相连;
C.X含酚-OH,与溴水发生取代反应,Y含碳碳双键、酚-OH,碳碳双键与溴水发生加成反应;
D.Y中碳碳双键、苯环、羰基均与氢气发生加成反应.
解答 解:A.X中含酚-OH,易被氧化,不能在空气中稳定存在,故A错误;
B.苯环、羰基为平面结构,且二者直接相连,则X中所有碳原子可处于同一平面,故B正确;
C.X含酚-OH,与溴水发生取代反应,Y含碳碳双键、酚-OH,碳碳双键与溴水发生加成反应,则X不能与溴水发生加成反应,故C错误;
D.Y中碳碳双键、苯环、羰基均与氢气发生加成反应,则1 mol化合物Y最多可以与5 mol H2反应,故D错误;
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意烯烃、酚的性质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用铂丝蘸取某盐溶液进行焰色反应,火焰呈黄色,说明该盐溶液含钠元素,一定不含钾元素 | |
| B. | 用小刀切下一小块金属钠,将剩余的钠再放回原试剂瓶 | |
| C. | 向某溶液中加入BaCl2溶液产生白色沉淀,再加稀盐酸沉淀不溶解,说明原溶液中一定含有SO42- | |
| D. | 向沸水中逐滴滴加1mol•L-1FeCl3溶液,并不断用玻璃棒搅拌,可制得Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增加H2的浓度,可提高CO2转化率 | |
| B. | 升高温度,可提高CO2转化率 | |
| C. | 升高温度,正反应速率减小,逆反应速率增加,平衡逆向移动 | |
| D. | 改用高效催化剂,可增大反应的平衡常数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①反应:CH2=CH2+H2O $\stackrel{催化剂}{→}$ CH3CH2OH取代反应 | |
| B. | ②反应:CH3CH2OH+O2$→_{△}^{Cu}$ CH3CHO+H2O氧化反应 | |
| C. | ③反应:2 CH3CHO+O2$\stackrel{催化剂}{→}$ 2CH3COOH氧化反应 | |
| D. | ④反应:CH3COOH+C2H5OH $→_{△}^{浓硫酸}$ CH3COOC2H5加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| B. | 钠具有强还原性,可用于制作高压钠灯 | |
| C. | 漂白粉在空气中不稳定,可用于漂白纸张 | |
| D. | 氢氧化铝受热易分解,可用作胃酸中和剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 西维因分子式为C12H10NO2 | |
| B. | 西维因苯环上一溴取代产物有4种情况 | |
| C. | 可用FeCl3溶液检验西维因是否发生水解 | |
| D. | 在Ni催化下lmol西维因最多能与6molH2加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
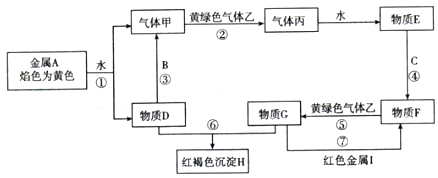
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com