
【题目】根据有机化合物的命名原则,下列命名正确的是
A.![]() 3-甲基-1,3-丁二烯
3-甲基-1,3-丁二烯
B.![]() 2-羟基丁烷
2-羟基丁烷
C.CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷
D.(CH3)3CCl 2-甲基-2-氯丙烷
科目:高中化学 来源: 题型:
【题目】根据元素周期表中完整周期元素的性质,完成下列空格。
(1)在第三周期中,第一电离能最小的元素符号是________,其原子的结构示意图为__________,第一电离能最大的元素符号是________,其价电子排布式为___________________________。
(2)在元素周期表中,电负性最大的元素名称是________,其价电子排布图为______________
(3)第四周期元素中未成对电子数最多的元素符号是________,其原子的简化电子排布式为__________,有_____个未成对电子,有_____个能级,能量最高的能级符号为_______。
(4)某元素的基态原子价电子排布式为3d104s1 ,该元素符号是_________,原子中所有电子占有________个轨道,核外共有________个不同运动状态的电子。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. ![]() 分子中的所有原子有可能共平面
分子中的所有原子有可能共平面
B. ![]() 中有8个碳原子可能在同一条直线上
中有8个碳原子可能在同一条直线上
C. 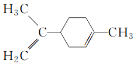 所有碳原子一定在同一平面上
所有碳原子一定在同一平面上
D. ![]() 至少有16个原子共平面
至少有16个原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是核电荷数依次增大的五种短周期主族元素,A元素的原子核内只有1个质子;B元素的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层多4;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C;C、E同主族。
(1)E元素形成的氧化物对应的水化物的化学式为_______________________________。
(2)元素C、D、E形成的简单离子半径大小关系是____________(用离子符号表示)。
(3)用电子式表示化合物D2C的形成过程:_________________。C、D还可形成化合物D2C2,D2C2中含有的化学键类型是_______________________________________________。
(4)由A、B、C三种元素形成的离子化合物的化学式为__________________,它与强碱溶液共热,发生反应的离子方程式是______________________。
(5)某一反应体系中含有D2E、D2EC3、D2EC4三种物质,若此反应为分解反应,则此反应的化学方程式为________________________(化学式用具体的元素符号表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为氢氧燃料电池装置示意图,下列有关说法正确的是( )
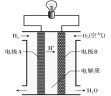
A. 电极A为正极
B. 产物为水,属于环境友好电池
C. 电子流向:电极B→导线→电极A
D. 该电池的化学能可以100%转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应N2+3H2![]() 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是( )
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是( )
A. 3v正(N2)=v正(H2)B. v正(N2)=v逆(NH3)
C. 2v正(H2)=3v逆(NH3)D. v正(N2)=3v逆(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素单质可以参与很多化学反应, 如:NF3气体可由NH3和F2在Cu催化剂存在下反应直接得到;反应①:2NH3+3F2![]() NF3+ 3NH4F,Ta(钽)是一种过渡元素,利用“化学蒸气转移法”可以制备TaS2晶体;反应②:TaI4(g)+S2(g)
NF3+ 3NH4F,Ta(钽)是一种过渡元素,利用“化学蒸气转移法”可以制备TaS2晶体;反应②:TaI4(g)+S2(g)![]() TaS2(s)+2I2(g)+QkJ,Q>0
TaS2(s)+2I2(g)+QkJ,Q>0
(1)反应①中:非金属性最强的元素原子核外有____种不同运动状态的电子;该反应中的某元素的单质可作粮食保护气,则该元素最外层的电子有___种自旋方向。
(2)反应①中:物质所属的晶体类型有____;并写出所有原子符合8电子稳定结构的化合物的电子式____。
(3)反应②中:平衡常数表达式:K=___,若反应达到平衡后,保持其他条件不变,降低温度,重新达到平衡时____。
a.平衡常数K增大 b. S2的浓度减小 c. I2的质量减小 d. V(TaI4)逆 增大
(4)反应②在一定温度下进行,若反应容器的容积为2L,3min后达到平衡,测得蒸气的质量减少了2.45g,则I2的平均反应速率为___。
(5)某同学对反应②又进行研究,他查阅资料,发现硫单质有多种同素异形体,可表示Sx(x为偶数),且在一定条件下可以相互转化,他认为仅增大压强对平衡是有影响的,则TaI4的平衡转化率会____(填增大或减小),其原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】膳食纤维具有突出的保健功能,是人体的“第七营养素”。木质素是一种非糖类膳食纤维,其单体之一是芥子醇,结构简式如图所示。下列有关芥子醇的说法正确的是( )
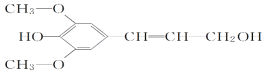
A. 芥子醇的分子式是C11H14O4,属于芳香烃
B. 1 mol芥子醇与足量浓溴水反应,最多消耗3 mol Br2
C. 芥子醇不能与FeCl3溶液发生显色反应
D. 芥子醇能发生的反应类型有氧化反应、取代反应、加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置示意图和有关数据如下:
![]()
项目 | 相对分子质量 | 密度/(g·cm3) | 沸点/℃ | 水中溶解性 |
异戊醇 | 88 | 0.812 3 | 131 | 微溶 |
乙酸 | 60 | 1.049 2 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.867 0 | 142 | 难溶 |
![]()
实验步骤:
在A中加入4.4 g异戊醇、6.0 g乙酸、数滴浓硫酸和2~3片碎瓷片,开始缓慢加热A50 min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯3.9 g。
回答下列问题:
(1)仪器B的作用是________________。
(2)在洗涤操作中,第一次水洗的主要目的是____________________,第二次水洗的主要目的是________________________________________。
(3)在洗涤、分液操作中,应充分振荡,然后静置,待分层后________(填标号)。
a.直接将乙酸异戊酯从分液漏斗的上口倒出
b.直接将乙酸异戊酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从下口放出
d.先将水层从分液漏斗的下口放出,再将乙酸异戊酯从上口倒出
(4)本实验中加入过量乙酸的目的是________________________;加入少量无水MgSO4的目的是__________________。
(5)在蒸馏操作中,仪器选择及安装都正确的是________(填标号)。
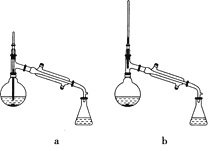
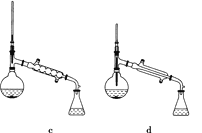
(6)在进行蒸馏操作时,若从130 ℃便开始收集馏分,会使实验的产率偏________(填“高”或“低”),其原因是_____________________________________________________。
(7)本实验的产率是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com