
| A.15.12 L | B.10.08 L | C.2.24 L | D.3.36 L |
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源:不详 题型:单选题
| A.m1一定大于m2 | B.m1可能等于m2 |
| C.m1一定等于m2 | D.m1可能大于m2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
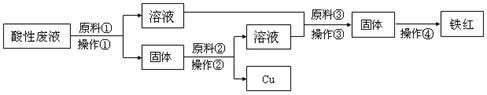
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
| 实验步骤 | 实验操作 | 实验操作的目的 |
| 步骤1 | | |
| 步骤2 | | |
| 步骤3] | | |
| 步骤4 | 洗涤 | |
| 步骤5 | | 得到FeSO4溶液 |
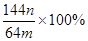 。该学生的计算是否正确: ,请说明理由 。
。该学生的计算是否正确: ,请说明理由 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 6SO2+Fe3O4,有3 molFeS2参加反应,转移 mol电子
6SO2+Fe3O4,有3 molFeS2参加反应,转移 mol电子查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。
Fe2(SO4)3 + 3SO2↑+ 6H2O。请你参与探究并回答相关问题。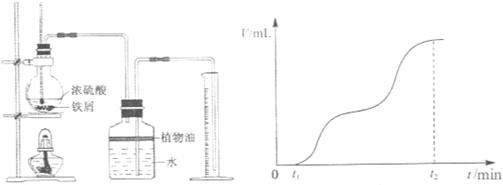
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com