
【题目】已知: 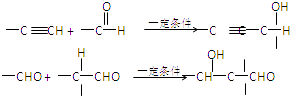 以乙炔为原料,通过如图所示步骤能合成有机物中间体E(转化过程中的反应条件及部分产物已略去).
以乙炔为原料,通过如图所示步骤能合成有机物中间体E(转化过程中的反应条件及部分产物已略去). ![]()
其中,A、B、C、D分别代表一种有机物;B的化学式为C4H10O2 , 分子中无甲基.
请回答下列问题:
(1)A→B的化学反应类型是 .
(2)写出生成A的化学方程式: .
(3)B在浓硫酸催化下加热,可生成多种有机物.写出2种相对分子质量比A小的有机物的结构简式:、 .
(4)写出C生成D的化学方程式: .
(5)含有苯环,且与E互为同分异构体的酯有种,写出其中二种同分异构体的结构简式: .
【答案】
(1)加成反应
(2)![]()
(3)CH2=CH﹣CH2CH2OH;CH2=CH﹣CH=CH2
(4)
(5)5;![]() 、
、 ![]() 等
等
【解析】解:根据乙炔与B的分子式C4H10O2 , 结合反应信息可知,乙炔 ![]() A是1分子乙炔与2分子甲醛发生加成反应,则A为HOCH2C≡CCH2OH,HOCH2C≡CCH2OH与氢气发生加成反应生成B,B为HOCH2CH2CH2CH2OH,由E的结构,结合反应信息可知,HOCH2CH2CH2CH2OH氧化生成的C,C为OHCCH2CH2CHO,C发生给出的信息中的反应生成D,D为
A是1分子乙炔与2分子甲醛发生加成反应,则A为HOCH2C≡CCH2OH,HOCH2C≡CCH2OH与氢气发生加成反应生成B,B为HOCH2CH2CH2CH2OH,由E的结构,结合反应信息可知,HOCH2CH2CH2CH2OH氧化生成的C,C为OHCCH2CH2CHO,C发生给出的信息中的反应生成D,D为 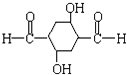 ,再发生消去反应生成E,(1)根据乙炔与B的分子式C4H10O2 , 结合反应信息可知,乙炔
,再发生消去反应生成E,(1)根据乙炔与B的分子式C4H10O2 , 结合反应信息可知,乙炔 ![]() A是1分子乙炔与2分子甲醛发生加成反应, 所以答案是:加成反应;(2)由信息可知,乙炔中A原子活泼,与醛发生加成反应,醛基中C=O双键中其中1个键断裂,乙炔中A原子连接醛基中O原子,乙炔中C原子与醛基中C原子连接,根据乙炔与B的分子式C4H10O2可知,乙炔
A是1分子乙炔与2分子甲醛发生加成反应, 所以答案是:加成反应;(2)由信息可知,乙炔中A原子活泼,与醛发生加成反应,醛基中C=O双键中其中1个键断裂,乙炔中A原子连接醛基中O原子,乙炔中C原子与醛基中C原子连接,根据乙炔与B的分子式C4H10O2可知,乙炔 ![]() H是1分子乙炔与2分子甲醛发生加成反应,A为HOCH2C≡CCH2OH,反应方程式为
H是1分子乙炔与2分子甲醛发生加成反应,A为HOCH2C≡CCH2OH,反应方程式为 ![]() ,
,
所以答案是: ![]() ;(3)HOCH2C≡CCH2OH与氢气发生加成反应生成B为HOCH2CH2CH2CH2OH,在浓硫酸催化下加热,羟基发生消去反应(或成环状醚键)生成的物质比A的相对分子质量小,符合条件有:CH2=CH﹣CH2CH2OH、CH2=CH﹣CH=CH2、
;(3)HOCH2C≡CCH2OH与氢气发生加成反应生成B为HOCH2CH2CH2CH2OH,在浓硫酸催化下加热,羟基发生消去反应(或成环状醚键)生成的物质比A的相对分子质量小,符合条件有:CH2=CH﹣CH2CH2OH、CH2=CH﹣CH=CH2、 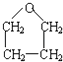 ,所以答案是:CH2=CH﹣CH2CH2OH;CH2=CH﹣CH=CH2;(4)由E的结构,结合反应信息可知,HOCH2CH2CH2CH2OH氧化生成的C为OHCCH2CH2CHO,C发生给出的信息中的反应生成D为
,所以答案是:CH2=CH﹣CH2CH2OH;CH2=CH﹣CH=CH2;(4)由E的结构,结合反应信息可知,HOCH2CH2CH2CH2OH氧化生成的C为OHCCH2CH2CHO,C发生给出的信息中的反应生成D为 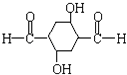 ,故C生成D的化学方程式为
,故C生成D的化学方程式为  ,所以答案是:
,所以答案是:  ;(5)含有苯环,且与E互为同分异构体的酯,结合E的结构可知,该同分异构体中含有1个酯基、1个苯环,若侧链只有1个取代基,可以为﹣OOCCH3、﹣COOCH3、﹣CH3OOCH,若侧链含有2个取代基,为﹣CH3、﹣OOCH,有邻、间、对三种位置关系,故符合条件的同分异构体由3+3=6种,结构简式为:
;(5)含有苯环,且与E互为同分异构体的酯,结合E的结构可知,该同分异构体中含有1个酯基、1个苯环,若侧链只有1个取代基,可以为﹣OOCCH3、﹣COOCH3、﹣CH3OOCH,若侧链含有2个取代基,为﹣CH3、﹣OOCH,有邻、间、对三种位置关系,故符合条件的同分异构体由3+3=6种,结构简式为: 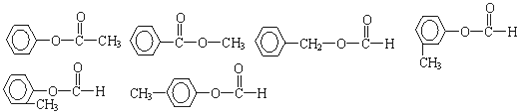 ,所以答案是:
,所以答案是: ![]() 、
、 ![]() 等.
等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列有关用标准盐酸滴定未知浓度氨水的实验操作叙述正确的是
A.锥形瓶用待测液润洗
B.酸式滴定管用标准液润洗
C.临近滴定终点时眼睛须注视酸式滴定管刻度线
D.记录一次滴定实验结果即可处理数据
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CO合成甲醇的化学方程式为:CO(g)+2H2(g)CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( ) 
A.温度:T1>T2>T3
B.正反应速率:υ(a)>υ(b)>υ(c)
C.平衡常数:K(b)>K(d)
D.CH3OH的体积分数(a)>(b)>(c)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个固定容积的密闭容器中充入2molNO2 , 一定温度下建立如下平衡:2NO2 ![]() N2O4 , 此时平衡混合气中NO2的体积分数为x%,若再充入1mol N2O4 , 在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是( )
N2O4 , 此时平衡混合气中NO2的体积分数为x%,若再充入1mol N2O4 , 在温度不变的情况下,达到新的平衡时,测得NO2的体积分数为y%,则x和y的大小关系正确的是( )
A.x>y
B.x<y
C.x=y
D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明强酸性溶液中,能大量共存的离子组是( )
A. K+、Cu2+、NO3﹣、SO42﹣ B. K+、Na+、Cl﹣、ClO﹣
C. Zn2+、NH4+、NO3﹣、Cl﹣ D. K+、Na+、Ba2+、SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.溶液中水的离子积常数(KW)随溶液浓度的改变而改变
B.一般情况下,一元弱酸HA的Ka越大,表明该酸的酸性越弱
C.对已达到化学平衡的反应,改变压强,平衡常数(K)一定改变
D.Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】10mL NO、CO2的混合气体通过足量的Na2O2后,气体的体积变为5mL(相同状况),则CO2和NO的体积比不可能为( )
A.1:1
B.2:1
C.3:2
D.1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaCl、NaOH、Na2CO3和NaHCO3均是重要的化工原料,相互间可以发生转化,请回答以下问题:

(1)粗盐经溶解、过滤和蒸发操作后,仍含有MgCl2及Na2SO4等可溶性杂质,请写出检验其中是否含有![]() 的离子方程式:____________________________。
的离子方程式:____________________________。
(2)实验室要配制480mL0.2mol/L的NaOH溶液,需要称量NaOH固体的质量为__________g。
(3)如图,实验一是为了比较Na2CO3和NaHCO3的热稳定性,则试管A中所盛的药品为____________(填化学式),能证明热稳定性强弱的现象为_____________,试管中发生反应的化学方程式为_______________。
(4)实验二是为了探究Na2O2与CO2的反应,写出该反应的化学方程式___________________。
(5)向饱和的Na2CO3溶液中通入CO2的现象为____________________________________,写出发生反应的离子方程式______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
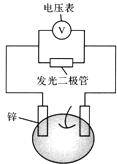
【题目】留心处处皆学问.从生活出发进行科学探究,可以获得自信,形成正确的思维方式.甲、乙两位同学一起合作设计完成了水果电池的实验(如图),测得数据如下
实验序号 | 电极材料 | 水果种类 | 电极间距离/cm | 电压/mV |
1 | 锌铜 | 菠萝 | 3 | 900 |
2 | 锌铜 | 苹果 | 3 | 650 |
3 | 锌铜 | 柑橘 | 3 | 850 |
4 | 锌铜 | 西红柿 | 3 | 750 |
5 | 锌铝 | 菠萝 | 3 | 650 |
6 | 锌铝 | 苹果 | 3 | 450 |
对甲同学提出的问题,乙同学的解释不正确的是( )
甲同学 | 乙同学 | |
A | 实验6中负极电极反应式如何写? | Al﹣3e﹣=Al3+ |
B | 实验1,5中电流方向为什么相反? | 1中锌为负极,电流由铜经导线流向锌,5中铝为负极,铝失去电子,电流由锌经导线流向铝 |
C | 水果电池的电压与哪些因素有关? | 只跟水果的类型有关 |
D | 实验中发光二极管不亮,如何使它亮起来 | 可用铜锌作电极,用菠萝作介质,并将多个此电池串联起来 |
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com