
| 实验事实 | 结论 | |
| ① | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| ② | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| ③ | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| ④ | 常温下白磷自燃而氮气在放电时才与氧气反应 | 非金属性:P>N |
| ⑤ | 某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定有NH4+ |
| A. | ①②③ | B. | ①③⑤ | C. | ②③⑤ | D. | ③④⑤ |
分析 ①品红溶液褪色,气体可能具有漂白性或气体与水反应的物质具有漂白性;
②Mg与二氧化碳反应生成MgO和C,Mg元素的化合价升高;
③白色沉淀为氢氧化铝,偏铝酸根离子促进碳酸氢根离子的电离;
④常温下白磷自燃而氮气在放电时才与氧气反应,与物质中的化学键有关,N≡N键能大;
⑤能使湿润红色石蕊试纸变蓝的气体为氨气.
解答 解:①品红溶液褪色,气体可能具有漂白性或气体与水反应的物质具有漂白性,则气体为SO2、Cl2等,故错误;
②Mg与二氧化碳反应生成MgO和C,Mg元素的化合价升高,Mg作还原剂,还原剂的还原性大于还原产物的还原性,则还原性Mg>C,故正确;
③白色沉淀为氢氧化铝,偏铝酸根离子促进碳酸氢根离子的电离,则酸性:HCO3->Al(OH)3,故正确;
④常温下白磷自燃而氮气在放电时才与氧气反应,与物质中的化学键有关,N≡N键能大,而非金属性N>P,故错误;
⑤能使湿润红色石蕊试纸变蓝的气体为氨气,由操作和现象可知,该溶液一定有NH4+,故正确;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及气体的性质、氧化还原反应、酸性比较、离子检验等,把握物质的性质及反应原理为解答的关键,侧重分析与应用能力的考查,注意实验的评价性分析,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液中滴加浓氨水至过量:Al3++4NH3•H2O=AlO2-+4NH4++2H2O | |
| B. | MnO2与浓盐酸反应制取Cl2:MnO2+4H++4Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2Cl2↑+2H2O | |
| C. | 小苏打溶液中加入足量稀盐酸:HCO3-+H+=CO2↑+H2O | |
| D. | 电解饱和食盐水的阴极反应:2Cl--2e-=Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
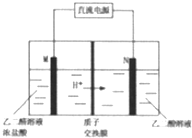 乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法不正确的是( )
乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法不正确的是( )| A. | N电极上的电极反应式:HOOC-COOH+2e-+2H+═HOOC-CH0+H2O | |
| B. | 若有2molH+通过质子交换膜并完全参与反应,则该装置中生成的乙醛酸为1mol | |
| C. | M电极上的电极反应式为:2Cl--2e-═Cl2↑ | |
| D. | 乙二醛与M电极的产物反应生成乙醛酸的化学方程式:Cl2+OHC-CHO+H2O═HOOC-CHO+2HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 四种元素中,元素Z的非金属性最强 | |
| B. | X、Y、Z三种元素不可能形成离子化合物 | |
| C. | Y、Z、W三种元素的原子半径大小顺序:r(Z)>r(W)>r(Y) | |
| D. | YW3、ZW2、Z2W2中各原子最外层均达到8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y元素最高价氧化物对应水化物化学式H2YO4 | |
| B. | 原子半径由大到小的顺序为:Y>Z>X | |
| C. | X与W形成的两种化合物中,阴、阳离子物质的量之比均为1:2 | |
| D. | X、Z两种元素的气态氢化物中,Z的气态氢化物较稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
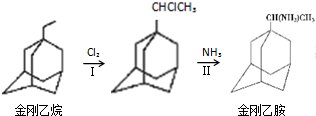
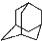 ,如金刚乙烷表示为R-CH2CH3);
,如金刚乙烷表示为R-CH2CH3);
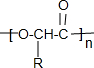 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 始祖鸟烯(Pterodactyladiene),形状宛如一只展翅飞翔的鸟,其键线式(线表示C-C键,端点、交点表示碳原子)如图,其中R1、R2为烷烃基.则下列有关始祖鸟烯的说法中正确的是( )
始祖鸟烯(Pterodactyladiene),形状宛如一只展翅飞翔的鸟,其键线式(线表示C-C键,端点、交点表示碳原子)如图,其中R1、R2为烷烃基.则下列有关始祖鸟烯的说法中正确的是( )| A. | 始祖鸟烯与乙烯互为同系物 | |
| B. | 若R1=R2=-CH3,则其化学式为C12H16 | |
| C. | 始祖鸟烯既能使酸性高锰酸钾褪色也能使溴水褪色,其褪色原理是一样的 | |
| D. | 若R1=R2,一定条件下烯烃双键碳原子上的氢也能取代,则始祖鸟烯环上的二氯代物有10种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com