
”¾ĢāÄæ”æĻĀĶ¼ĪŖÕż¶”ĶéµÄĒņ¹÷Ä£ŠĶ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ(””””)
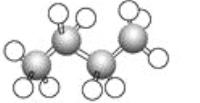
A. Õż¶”ĶéµÄ·Ö×ÓŹ½ĪŖC4H8
B. ·Ö×ÓÖŠ4øöĢ¼Ō×ÓŌŚĶ¬Ņ»ĢõÖ±ĻßÉĻ
C. ·Ö×ÓÖŠŗ¬ÓŠ4øöC”ŖCµ„¼ü
D. ·Ö×ÓÖŠ¹²ŗ¬ÓŠ13øö¹²¼Ū¼ü
”¾“š°ø”æD
”¾½āĪö”æ·ÖĪö:ÓÉÕż¶”ĶéµÄĒņ¹÷Ä£ŠĶæÉŅŌŠ“³öĘä·Ö×ÓŹ½ĪŖC4H10£¬·Ö×ÓÖŠ4øöĢ¼Ō×ÓŠĪ³ÉµÄĢ¼Į“ĪŖ¾ā³Ż×“£»·Ö×ÓÖŠµÄ4øöĢ¼Ō×ÓŠĪ³É3øöC”ŖCµ„¼ü£¬10øöĒāŌ×ÓŠĪ³É10øöC”ŖHµ„¼ü£¬¹²ŠĪ³É13øö¹²¼Ū¼ü”£
ÓÉÕż¶”ĶéµÄĒņ¹÷Ä£ŠĶæÉŅŌŠ“³öĘä·Ö×ÓŹ½ĪŖC4H10£¬ŹōÓŚĶéĢž£¬A“ķĪó£»¼×Ķé·Ö×ÓĪŖÕżĖÄĆęĢå¹¹ŠĶ£¬Ņņ“ĖøĆ·Ö×ÓÖŠ4øöĢ¼Ō×ÓŠĪ³ÉµÄĢ¼Į“ĪŖ¾ā³Ż×“£¬²»æÉÄÜ4øöĢ¼Ō×ÓŌŚĶ¬Ņ»ĢõÖ±ĻßÉĻ£¬B“ķĪó£»øł¾ŻÕż¶”ĶéµÄĒņ¹÷Ä£ŠĶæÉŅŌÖŖµĄ£¬·Ö×ÓÖŠŗ¬ÓŠ3øöC”ŖCµ„¼ü£¬C“ķĪó£»ĒāŌ×ÓÓėĢ¼Ō×Ó¼äŠĪ³É10Ģõ¹²¼Ū¼ü£¬Ģ¼Ģ¼Ō×Ó¼äŠĪ³É3Ģõ¹²¼Ū¼ü£¬¹²¼Ęŗ¬ÓŠ13øö¹²¼Ū¼ü£¬DÕżČ·£»ÕżČ·Ń”ĻīD”£
µć¾¦;¼×ĶéŹĒ×ī¼ņµ„µÄĶéĢž£¬ÓÉÓŚ¼×ĶéĪŖÕżĖÄĆęĢå½į¹¹£¬Ņņ“ĖĶéĢžµÄ½į¹¹ÖŠ£¬Ļąµ±ÓŚŗ¬ÓŠ-CH3”¢ -CH2- ”¢ ![]() ”¢
”¢![]() ½į¹¹£¬ĖłŅŌĶéĢž¾łĪŖæռ乹ŠĶ£¬²»ŹĒĘ½Ćę¹¹ŠĶ”£
½į¹¹£¬ĖłŅŌĶéĢž¾łĪŖæռ乹ŠĶ£¬²»ŹĒĘ½Ćę¹¹ŠĶ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æSO2ŗĶNOxŹĒ“óĘųĪŪČ¾ĪļµÄÖ÷ŅŖ³É·Ö”£·ĄÖ¹æÕĘųĪŪČ¾£¬±£ĪĄ”°Ą¼ÖŻĄ¶”±ŹĒĄ¼ÖŻŹŠŅ»ĻīÖŲŅŖĆńÉś¹¤³Ģ”£ĄūÓĆĻĀĶ¼ĖłŹ¾×°ÖĆ(µē¼«¾łĪŖ¶čŠŌµē¼«)æÉŅŌĪüŹÕSO2»¹æÉŅŌÓĆŅõ¼«ÅųöµÄČÜŅŗĪüŹÕNO2”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
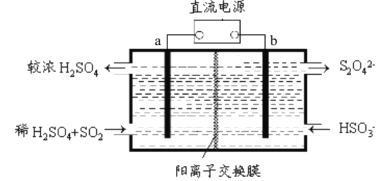
A. µē¼«aÓ¦Į¬½ÓµēŌ“µÄÕż¼«
B. µē¼«bÉĻµÄµē¼«·“Ó¦Ź½ĪŖ2HSO3-+2e-+2H+=S2O42-+2H2O
C. ·“Ó¦¹ż³ĢÖŠ£¬H+“Óa¼«ŹŅĮ÷Ļņb¼«ŹŅ
D. ĆæĪüŹÕ±źæöĻĀ22.4LSO2£¬ŌŚb¼«ŹŅÉś³É2NAøöS2O42-
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æij»ÆѧŠ”×éŃŠ¾æŌŚĘäĖūĢõ¼ž²»±äŹ±£¬øıäĆܱÕČŻĘ÷֊ijŅ»Ģõ¼ž¶ŌA2£Øg£©+3B2£Øg£©2AB3£Øg£©»ÆŃ§Ę½ŗāדĢ¬µÄÓ°Ļģ£¬µĆµ½ČēĶ¼ĖłŹ¾µÄĒśĻߣØĶ¼ÖŠT±ķŹ¾ĪĀ¶Č£¬n±ķŹ¾ĪļÖŹµÄĮ棩ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£© 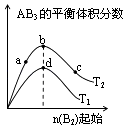
A.Ķ¼ÖŠT2Ņ»¶Ø“óÓŚT1
B.Ķ¼ÖŠbµćĖŁĀŹŅ»¶Ø“óÓŚdµćĖŁĀŹ
C.“ļµ½Ę½ŗāŹ±£¬A2µÄ×Ŗ»ÆĀŹ“óŠ”ĪŖ£ŗc£¾b£¾a
D.¼ÓČė“߻ƼĮæÉŅŌŹ¹×“Ģ¬d±äĪŖדĢ¬b
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æI.2Al+Fe2O3![]() Al2O3+2FeŌŚ»Æѧ·“Ó¦¹ż³ĢÖŠ²śÉś³¬øßČČ£¬ŌųÓĆÓŚøÖ¹ģŗø½Ó”£Ķź³ÉĻĀĮŠĢīæÕ£ŗ
Al2O3+2FeŌŚ»Æѧ·“Ó¦¹ż³ĢÖŠ²śÉś³¬øßČČ£¬ŌųÓĆÓŚøÖ¹ģŗø½Ó”£Ķź³ÉĻĀĮŠĢīæÕ£ŗ
£Ø1£©ŃõŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ_______________£¬ĘäĄė×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ__________”£
£Ø2£©ĀĮŃĪ³£ÓĆ×÷¾»Ė®¼Į£¬ÓĆĪÄ×ÖŗĶ»ÆѧÓĆÓļ½ųŠŠ½āŹĶ_______________________________”£
£Ø3£©ŃõµÄ·Ē½šŹōŠŌĒæÓŚµŖ£¬ÓĆŌŖĖŲÖÜĘŚĀÉÖŖŹ¶·ÖĪöŌŅņ_____________________________”£
£Ø4£©Al2O3ÓėNaOHČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ______________________________________”£
II.NH4Al(SO4)2”¤12H2OĖ®ČÜŅŗ³Ź_____ŠŌ£ØŃ”Ģī”°Ėį”±”¢”°¼ī”±»ņ”°ÖŠ”±£©£¬±Č½ĻČÜŅŗÖŠĄė×ÓÅØ¶Č“óŠ”c(NH4+)_____c(Al3+)£ØŃ”Ģī”°£¾”±”¢”°£¼”±»ņ”°=”±£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾£ØŅŅ×°ÖĆÖŠXĪŖŃōĄė×Ó½»»»Ä¤£¬¼×ĆŃµÄ½į¹¹¼ņŹ½ĪŖCH3OCH3£© 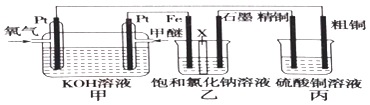
øł¾ŻŅŖĒó»Ų“šĻĀĮŠĻą¹ŲĪŹĢā£ŗ
£Ø1£©Š“³öøŗ¼«µÄµē¼«·“Ó¦£ŗ £®
£Ø2£©ĒāŃõ»ÆÄĘÖ÷ŅŖŌŚ£ØĢī”°Ģś¼«”±»ņ”°ŹÆÄ«¼«”±£©ĒųÉś³É£®
£Ø3£©Čē¹ū“ÖĶÖŠŗ¬ÓŠŠæ”¢ŅųµČŌÓÖŹ£¬Ōņ“ÖĶµÄµē¼«·“Ó¦ĪŖ£ŗ”¢ £®
£Ø4£©·“Ó¦Ņ»¶ĪŹ±¼ä£¬ĮņĖįĶČÜŅŗµÄÅØ¶Č½«£ØĢī”°Ōö“ó”±”¢”°¼õŠ””±»ņ”°²»±ä”±£©£®
£Ø5£©ČōŌŚ±ź×¼×“æöĻĀÓŠ2.24LŃõĘų²Ī¼Ó·“Ó¦£¬±ū×°ÖĆÖŠŅõ¼«Īö³öĶµÄÖŹĮæĪŖ £®
£Ø6£©Čō½«±ū×°ÖĆøijÉŌŚ±ź×¼×“æöĻĀ£¬ÓĆŹÆÄ«×÷µē¼«µē½āĢå»żĪŖ2LµÄCuSO4ČÜŅŗ£¬Š“³öµē½āCuSO4ČÜŅŗŹ±µÄĄė×Ó·“Ó¦·½³ĢŹ½£»µ±µē½āŹŹµ±Ź±¼äŗó¶ĻæŖµēŌ“£¬·¢ĻÖÖ»Šč²¹³ä22.2g¹ĢĢåCu2£ØOH£©2CO3¼“æÉŹ¹µē½āŅŗ»Öø“µ½ŌÅضČÓėĢå»ż£¬ŌņŌCuSO4ČÜŅŗµÄÅØ¶ČŹĒmol/L£»Čō½«±ūÉč¼Ę³ÉŌŚ¶Ę¼žÉĻ¶ĘĶµÄ×°ÖĆ£¬øĆČēŗĪøĶƣ¬ĒėÓĆ¼ņŅŖµÄÓļŃŌŠšŹö£ŗ £®
£Ø7£©Čō½«ŅŅÖŠµÄ½»»»Ä¤Č„µō£¬·¢ĻÖÖ»ÓŠH2ŅŻ³ö£¬ŌņŹŌŠ“³öŅŅ³ŲÖŠ·¢ÉśµÄ×Ü·“Ó¦£ŗ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ2A+B3C+4D·“Ó¦ÖŠ£¬±ķŹ¾øĆ·“Ó¦ĖŁĀŹ×īæģµÄŹĒ£Ø””””£©
A.v£ØA£©=0.5 mol/£ØLs£©
B.v£ØB£©=0.3 mol/£ØLs£©
C.v£ØC£©=0.8 mol/£ØLs£©
D.v£ØD£©=1 mol/£ØLs£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲŌŖĖŲŗĶ»ÆŗĻĪļµÄŠšŹöÕżČ·µÄŹĒ
A. ×é³ÉĻø°ūµÄŌŖĖŲ“ó¶ąŅŌĪŽ»śŃĪµÄŠĪŹ½“ęŌŚ
B. µ„ĢĒŹĒ²»ÄÜĖ®½āµÄĢĒ
C. Ļø°ūÖŠ°üĄØĢĒĄą”¢Ö¬·¾”¢µ°°×ÖŹ”¢ŗĖĖįŌŚÄŚµÄÓŠ»śĪļ¶¼ÄÜĪŖĻø°ūÉśĆü»ī¶ÆĢį¹©ÄÜĮæ
D. ŅȵŗĖŲ”¢µ°°×ÖŹ”¢Ö¬·¾µÄŗĻ³É¹ż³ĢÖŠŠčŅŖ¹©øųµŖŌ“
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠČĖČĻĪŖŌŚŌŖĖŲÖÜĘŚ±ķÖŠ£¬Ī»ÓŚ¢ńA×åµÄĒāŌŖĖŲ£¬Ņ²æÉŅŌ·ÅŌŚ¢÷A×壬ĻĀĮŠĪļÖŹÄÜÖ§³ÖÕāÖÖ¹ŪµćµÄŹĒ
A.NaHB.H2OC.HClD.HClO
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒāÄÜŹĒŅ»ÖÖøߊ§Ēå½ą”¢¼«¾ß·¢Õ¹Ē±Į¦µÄÄÜŌ“”£ĄūÓĆÉśĪļÖŹ·¢½ĶµĆµ½µÄŅŅ“¼ÖĘČ”ĒāĘų£¬¾ßÓŠĮ¼ŗƵÄÓ¦ÓĆĒ°¾°”£
ŅŃÖŖĻĀĮŠ·“Ó¦£ŗ

(1)·“Ó¦¢ńŗĶ·“Ó¦¢ņµÄĘ½ŗā³£ŹżĖęĪĀ¶Č±ä»ÆĒśĻßČēĶ¼ĖłŹ¾”£Ōņ”÷H1________”÷H2(Ģī”°>”±”¢”°<”±»ņ”°=”±)£»”÷H3=________(ÓĆ”÷H1”¢”÷H2±ķŹ¾)”£
(2)Ļņ2LĆܱÕČŻĘ÷ÖŠ³äČėH2ŗĶCO2¹²6mol£¬øıäĒāĢ¼±Č[n(H2)/n(CO2)]ŌŚ²»Ķ¬ĪĀ¶ČĻĀ·¢Éś·“Ó¦III“ļµ½Ę½ŗāדĢ¬£¬²āµĆµÄŹµŃ鏿¾ŻČēĻĀ±ķ”£·ÖĪö±ķÖŠŹż¾Ż»Ų“šĻĀĮŠĪŹĢā£ŗ

¢ŁĪĀ¶ČÉżøߣ¬KÖµ________(Ģī”°Ōö“ó”±”¢”°¼õŠ””±”¢»ņ”°²»±ä”±)”£
¢ŚĢįøßĒāĢ¼±Č£¬KÖµ________ (Ģī”°Ōö“ó”±”°¼õŠ””±»ņ”°²»±ä”±)£¬¶ŌÉś³ÉŅŅ“¼________ (Ģī”°ÓŠĄū”±»ņ”°²»Ąū”±)
¢ŪŌŚ700K”¢ĒāĢ¼±ČĪŖ1.5£¬Čō5min·“Ó¦“ļµ½Ę½ŗāדĢ¬£¬Ōņ0~5minÓĆH2±ķŹ¾µÄĖŁĀŹĪŖ________”£
(3)·“Ó¦IIIŌŚ¾CO2±„ŗĶ“¦ĄķµÄKHCO3µē½āŅŗÖŠ£¬µē½ā»ī»ÆCO2ÖʱøŅŅ“¼µÄŌĄķČēĶ¼ĖłŹ¾”£

¢ŁŅõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ________________”£
¢Ś“Óµē½āŗóČÜŅŗÖŠ·ÖĄė³öŅŅ“¼µÄ²Ł×÷·½·ØĪŖ________________”£
(4)ŌŚŅ»¶ØĢõ¼žĻĀ·¢Éś·“Ó¦¢ō£¬²āµĆ²»Ķ¬ĪĀ¶Č¶ŌCO2µÄĘ½ŗā×Ŗ»ÆĀŹ¼°“߻ƼĮµÄŠ§ĀŹÓ°ĻģČēĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄĪŖ________ (ĢīŠņŗÅ)

¢Ł²»Ķ¬Ģõ¼žĻĀ·“Ó¦£¬NµćµÄĖŁĀŹ×ī“ó
¢ŚMµćĘ½ŗā³£Źż±ČNµćĘ½ŗā³£Źż“ó
¢ŪĪĀ¶ČµĶÓŚ250”ꏱ£¬ĖęĪĀ¶ČÉżøßŅŅĻ©µÄ²śĀŹŌö“ó
¢ÜŹµ¼Ź·“Ó¦Ó¦¾”æÉÄÜŌŚ½ĻµĶµÄĪĀ¶ČĻĀ½ųŠŠ£¬ŅŌĢįøßCO2µÄĘ½ŗā×Ŗ»ÆĀŹ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com