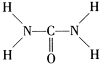
尿素(H
2NCONH
2)可用于制有机铁肥,主要代表有[Fe(H
2NCONH
2)
6](NO
3)
3[三硝酸六尿素合铁(Ⅲ)].
(1)基态Fe
3+的核外电子排布式为______.C、N、O三种元素的第一电离能由大到小的顺序是______.
(2)尿素分子中C、N原子的杂化方式分别是______.
(3)[Fe(H
2NCONH
2)
6](NO
3)
3中“H
2NCONH
2”与Fe(Ⅲ)之间的作用力是______.与NO
3-互为等电子体的一种化合物是______(写化学式).
(4)CO
2和NH
3是工业上制备尿素的重要原料,固态CO
2(干冰)的晶胞结构如图所示.
①1个CO
2分子周围等距离且距离最近的CO
2分子有______个.
②铜金合金的晶胞结构与干冰相似,若顶点为Au、面心为Cu,则铜金合金晶体中Au与Cu原子数之比为是______.




 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案