
| A. | 苯分子中C原子均以sp3杂化方式成键,形成夹角为120°的三个sp3杂化轨道,故为正六边形的碳环 | |
| B. | 每个碳原子还有一个未参与杂化的2p轨道,垂直碳环平面,相互交盖,形成大π键 | |
| C. | 大π键中6个电子被6个C原子共用,故称为6中心6电子大π键 | |
| D. | 苯分子中共有十二个原子共面,六个碳碳键完全相同 |
分析 在苯分子中,每个碳原子形成3个σ键,同时每个碳原子上未参与杂化的2p轨道形成大π键.6个碳碳键完全相同,键角皆为120°,苯分子中所有的碳碳之间的键均相同,是介于单键和双键之间的一种特殊类型的键,苯分子呈平面正六边形,据此分析解答.
解答 解:苯分子中,每个碳原子中的三个sp2杂化轨道分别与两个碳原子和一个氢原子形成3个σ键,同时每个碳原子还有一个未参加杂化的2p轨道,它们均有一个未成对电子,这些2p轨道相互平行,以“肩并肩”方式相互重叠,形成一个多电子的大π键,6个碳碳键完全相同,键角皆为120°,苯分子呈平面正六边形,分子中共有十二个原子共面,故A错误,BCD正确,
故选A.
点评 本题考查苯的化学键,注意苯分子中含有σ键和大π键,明确苯的结构即可解答,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2和CH4都是引起“温室效应”的气体 | |
| B. | Na2O、Na2O2的组成元素相同,但阳离子和阴离子的数目比不同 | |
| C. | SO2、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 分别向新制氯水和久置氯水中滴加少量紫色石蕊试液,充分振荡后溶液都呈红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
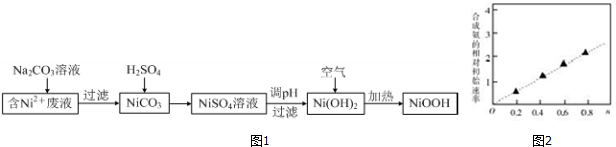
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 步骤 | 实验过程 | 实验用品 |
| I | 将干海带灼烧灰化 |  |
| II | 将海带灰溶解、过滤 |  和①玻璃棒 和①玻璃棒 |
| III | 氧化滤液中的I-,反应的离子方程式为②2I-+H2O2+2H+=I2+2H2O |  |
| IV | 取少量III中反应后溶液于试管中,加入少量CCl4并振荡后静置,观察到③下层溶液变为紫红色,说明海带中含有碘元素 |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Al2O3(熔融) $\frac{\underline{\;\;\;电解\;\;\;}}{冰晶石}$4Al+3O2↑ | |
| B. | Fe2O3+3CO $\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | |
| C. | Fe+CuSO4=FeSO4+Cu | |
| D. | 2NaCl(水溶液)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝与Fe2O3发生铝热反应后固体物质增重 | |
| B. | Al片溶于NaOH溶液,产生气体:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| C. | 工业上电解熔融状态的Al2O3制备Al | |
| D. | 铝制容器可盛装浓H2SO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com