
| 0.8g |
| 40g/mol |
|


科目:高中化学 来源: 题型:

| ①B2H6 |
| ②H2O2/OH- |
 →RCHO+H2O
→RCHO+H2O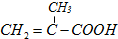 ,经过的反应是
,经过的反应是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C3H8O和C2H6O |
| B、C2H4和C3H8 |
C、 和C2H4 和C2H4 |
| D、CH2O和C2H4O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH相同的①CH3COONa、②NaClO、③NaHCO3、④NaOH四种溶液的c(Na+):④>②>③>① |
| B、0.1mol?L-1 HCl溶液与等体积0.05mol?L-1 Ba(OH)2溶液混合后,溶液中:n(H+)=n(OH-)=1.0×10-7mol |
| C、3.0L 0.1mol?L-1 NaOH溶液中缓慢通入CO2至溶液增重8.8g时,溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(H+) |
| D、浓度均为0.3mol?L-1的一元酸HY溶液与NaOH溶液等体积混合后,溶液的pH=9,则c(OH-)-c(HY)=c(H+)=1.0×10-9mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、当V<10mL时,c(HC2O4-)>c(OH-)>c(H+) |
| B、当V=10mL时,c(HC2O4-)>c(C2O42-))>c(H2C2O4) |
| C、当V=20mL时,c(K+)═2[c(C2O42-)+c(HC2O4-)] |
| D、当V>0,c(K+)+c(H+)=c(C2O)+c(HC2O4-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
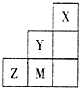
| A、非金属性:Y>Z>M |
| B、原子半径:M>Z>Y |
| C、气态氢化物的稳定性:HnY<HnM<HnZ |
| D、最高价氧化物相应水化物的酸性:HMOm>HnZOm |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、随着原子半径的增加,卤族元素单质的密度逐渐减小 |
| B、随着核电荷数的增加,卤族元素单质的熔点逐渐降低 |
| C、随着核电荷数的增加,卤族元素的原子半径逐渐减小 |
| D、随着原子半径的增加,卤族元素原子的非金属性逐渐减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com