
| A、①②③⑥ | B、②④⑤ |
| C、②④⑤⑥ | D、②④⑥ |


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
| 新制MnO2 |
| 25℃ |
| A、丙烯醇与丙醛(CH3CH2CHO)互为同分异构体 |
| B、丙烯醇含有两种官能团 |
| C、可用新制Cu(OH)2鉴别丙烯醛和丙烯醇 |
| D、此转化过程中丙烯醇被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:
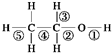
| A、乙醇和钠反应,键①断裂 |
| B、在Ag催化下和O2反应,键①③断裂 |
| C、乙醇和浓H2SO4共热140℃时,键①或键②断裂;在170℃时,键②⑤断裂 |
| D、乙醇完全燃烧时断裂键①② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该粒子不显电性 |
| B、与氢元素的质子数相同 |
| C、该粒子质量数为4 |
| D、该粒子质量比氢原子大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
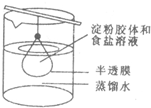 将10mL淀粉溶液和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图),2min后分别取袋内和烧杯内液体进行实验.下列说法正确的是( )
将10mL淀粉溶液和5mL氯化钠溶液混合后,放入用半透膜制成的袋内,将此袋浸入蒸馏水中(如图),2min后分别取袋内和烧杯内液体进行实验.下列说法正确的是( )| A、用激光笔照射该烧杯中的液体,会产生丁达尔现象 |
| B、烧杯内液体加入碘水后呈蓝色 |
| C、该淀粉胶体在催化剂作用下可水解生成葡萄糖和果糖 |
| D、将烧杯中液体蒸干,得到的固体物质可用来制取纯碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:
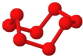
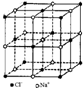
| 硼晶体的结构单元 | SF6分子 | S8分子 | NaCl | |
| 结构模型示意图 |  |
 |
 |
 |
| 备注 | 熔点1873K | / | 易溶于CS2 | / |
| A、单质硼属分子晶体,其结构单元B12中含有30个B-B键,含20个正三角形 |
| B、SF6是由极性键构成的分子 |
| C、固态硫S8属于原子晶体 |
| D、NaCl熔化和溶于水均能产生自由移动的离子,且破坏的是同种作用力,NaCl晶胞中每个Na+周围最近且等距离的Na+有6个 |
查看答案和解析>>
科目:高中化学 来源: 题型:
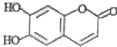 ,下列叙述不正确的是( )
,下列叙述不正确的是( )| A、该物质在酸性条件下加热可以水解 |
| B、1mol M最多能与3mol Br2发生反应 |
| C、M与足量的NaOH溶液发生反应时,所得有机产物的化学式为C9H4O5Na4 |
| D、1mol M与足量NaHCO3反应能生成2mol CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com