
 ��1��15.6g Na2X��Na+0.4moL����Na2X��Ħ������Ϊ
��1��15.6g Na2X��Na+0.4moL����Na2X��Ħ������Ϊ| m |
| n |
| m |
| n |
| 15.6g |
| 0.2mol |
| 0.02mol |
| 1mol/L |
| 0.04mol��1+0.02mol��3 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������¶����������������� |
| B�������¶�����ͭ�Ͽ췴Ӧ |
| C��¶���ڿ����У���Һ���������� |
| D��¶���ڿ����У���ҺŨ�Ⱦ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2HPO4����ˮ��Na2HPO4=2Na++H++PO43- |
| B��NaHSO4�ۻ���NaHSO4=Na++H++SO42- |
| C��HF��������ˮ�У�HF=H++F- |
| D����NH4��2SO4����ˮ����NH4��2SO4=2NH4++SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ʵ�����еĽ����ͨ��������ʢ��ú�͵��Լ�ƿ�У��Ա����������ˮ |
| B��150mL 1mol?L-1NaCl��Һ��75mL 1mol?L-1 NaHCO3��Һ��Na+���ʵ������ |
| C����FeCl3��Һ�еμ�KSCN��Һ�����Ѫ��ɫ���� |
| D���ýྻ�IJ�˿պȡ��Ʒ�ڻ��������տ�����ɫ���棬˵����Ʒ��һ������Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
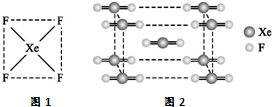 ���Դ�Ӣ����ѧ�Ұ����У�N��Bartlett���״κϳ��˵�һ��ϡ������Ļ�����XePtF6��������������̷�����믵�һϵ�л������XeF2��XeF4�ȣ�������Ϊ����ϡ�����廯ѧ��������ʷ�Թ��ף�
���Դ�Ӣ����ѧ�Ұ����У�N��Bartlett���״κϳ��˵�һ��ϡ������Ļ�����XePtF6��������������̷�����믵�һϵ�л������XeF2��XeF4�ȣ�������Ϊ����ϡ�����廯ѧ��������ʷ�Թ��ף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| NaOH/H2O |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� | |||||||||||||||||
| �� | �� | �� | |||||||||||||||
| �� | �� | �� | �� | ||||||||||||||
| �� | �� | ||||||||||||||||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com