
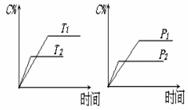
可逆反应a A(s)+b B(g)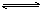 c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图下列叙述正确的是
c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图下列叙述正确的是
A.达平衡后,加入催化剂则C%增大
B.达平衡后,若升温,平衡左移
C.化学方程式中b <c +d
D.达平衡后,增加A的量有利于平衡向右移动
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
核内中子数为N的R2+的质量数为A,则n克它的氧化物所含质子 的物质的量是( )
的物质的量是( )
A.〔n(A-N+8) /(A+16)〕mol
/(A+16)〕mol
B.〔n(A-N+16)/(A+16)〕mol
C.〔n(A-N+8)/ A〕mol
D.〔n(A-N+16)/ A 〕mol
查看答案和解析>>
科目:高中化学 来源: 题型:
电解质的水溶液中存在电离平衡。
(1)醋酸是常见的弱酸。
① 醋酸在水溶液中的电离方程式为 。
② 下列方法中,可以使醋酸稀溶液中CH3COOH电离程度增大的是 (填字母序号)。
a.滴加少量浓盐酸 b.微热溶液
c.加水稀释 d.加入少量醋酸钠晶体
(2)用0.1 mol·L-1 NaOH溶液分别滴定体积均为20.00 mL、浓度均为0.1 mol·L-1的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
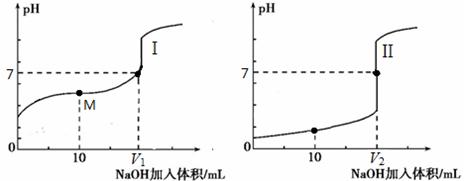
② 滴定醋酸的曲线是 (填“I”或“II”)。
② 滴定开始前,三种溶液中由水电离出的c(H+)最大的是 。
③ V1和V2的关系:V1 V2(填“>”、“=”或“<”)。
④ M点对应的溶液中,各离子的物质的量浓度由大到小的顺序是 。
(3)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验。
资料:AgSCN是白色沉淀,相同温度下,溶解度:AgSCN > AgI。
| 操作步骤 | 现象 |
| 步骤1:向2 mL 0.005 mol·L-1 AgNO3溶液中加入2 mL 0.005 mol·L-1 KSCN溶液,静置。 | 出现白色沉淀。 |
| 步骤2:取1 mL上层清液于试管中,滴加1滴2 mol·L-1 Fe(NO3)3溶液。 | 溶液变红色。 |
| 步骤3:向步骤2的溶液中,继续加入5滴3 mol·L-1 AgNO3溶液。 | 现象a ,溶液红色变浅。 |
| 步骤4:向步骤1余下的浊液中加入5滴3 mol·L-1 KI溶液。 | 出现黄色沉淀。 |
① 写出步骤2中溶液变红色的离子方程式 。
② 步骤3中现象a是 。
③ 用化学平衡原理解释步骤4的实验现象 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在足量锌与等物质的量浓度、等体积的盐酸和醋酸反应时,下列叙述正确的是
A.开始反应时,二者的速率相等 B.盐酸放出的H2多
C.二者放出的H2一样多 D.醋酸消耗的Zn的质量多
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下的固定容积的密闭容器中,当下列物理量不再变化时,表明反应:A(g)+2B(g) C(g)+D(g)已达到平衡状态
C(g)+D(g)已达到平衡状态
①混合气体的压强;②混合气体的密度;③各气体物质的物质量浓度;④气体的总物质的量;⑤混合气体的平均相对分子质量.
A.②③⑤ B.①②③ C.②③④⑤ D.①③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中微粒浓度关系一定正确的是( )
A.常温下,氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+ )
B.常温下,pH=2的一元酸和pH=12的一元强碱等体积混合: c(OH-)=c(H+)
C.0.1 mol·L—1的硫酸铵溶液中:c(NH4+ )>c(SO42 -)>c(H+)
D.0.1 mol·L—1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.某弱酸的酸式盐NaHA溶液中一定有:c(OH-)+2c(A2-)=c(H+)+c(H2A)
B.0.1 mol·L-1 CH3COONa 溶液与0.05 mol·L-1盐酸等体积混合后的酸性溶液中:
c(CH3COO-)>c(CH3COOH)>c(Cl-)>c(H+)
C.物质的量浓度相等的HCN溶液和NaCN溶液等体积混合后的溶液中:
c(CN-)+2c(OH-)=2c(H+)+c(HCN)
D.0.1 mol·L-1(NH4)2Fe(SO4)2溶液中:c(NH4+ )+c(NH3·H2O)+c(Fe2+)=0.3 mol·L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com