
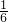 n(Fe2+)=0.0016 mol
n(Fe2+)=0.0016 mol 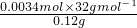 ×100%=90.7%
×100%=90.7% 

科目:高中化学 来源:101网校同步练习 高一化学 山东科学技术出版社 鲁教版 题型:022
据新华社报道:从2004年5月11日16日记者发稿时为止,广州市白云区“假酒中毒”事件中的死亡人数已增加到9人,住院人数增加到33人,其中10人病危.目前广州市有关部门查明:“毒酒”窝点有5桶工业酒精,每桶工业酒精的质量为165 kg,其中甲醇的质量分数为10%.饮用甲醇5 g-15 g即可使人中毒甚至死亡.据此消息:
(1)5桶工业酒精共含甲醇________kg这些甲醇若全被酒客饮用,死亡人数将继续上升,后果不堪设想.
(2)已知工业制备甲醇的方程式为:CO+2H2=x(x即为甲醇)由此可推断甲醇的化学式为________
(3)已知甲醇的分子结构和乙醇相似,根据结构决定性质的规律,请推测甲醇的一种化学性质:________
(4)认识到掌握化学知识能帮助人们抵御有害物质的侵害,由此我们联想到误食其它有害物质使人中毒的事件还有(请举一例)________
查看答案和解析>>
科目:高中化学 来源:海门市2007学年第一学期高三第一次诊断考试、化学试卷 题型:022
| |||||||||||
查看答案和解析>>
科目:高中化学 来源:英德中学2007届高三化学第二复习专题强化训练1 题型:022
| |||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)为了降低汽车尾气对大气的污染,有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。请写出表示甲醇燃烧的热化学方程式。
(2)测定工业甲醇中CH3OH的质量分数可按下法:取0.100 0 g工业甲醇样品,以适量H2SO4酸化后,加入20.00 mL 0.200 0 mol·L-1的K2Cr2O7溶液,过量的K2Cr2O7溶液,再用0.300 0 mol·L-1 (NH4)2Fe(SO4)2标准溶液滴定,耗去此标准液20.00 mL时,刚好到达滴定终点。
已知:CH3OH+![]() +8H+
+8H+![]() CO2↑+2Cr3++6H2O
CO2↑+2Cr3++6H2O
①写出H2SO4酸化的K2Cr2O7溶液与(NH4)2Fe(SO4)2溶液反应的离子方程式。
②求此工业甲醇中CH3OH的质量分数。
查看答案和解析>>
科目:高中化学 来源: 题型:
能源是人类社会发展进步的物质基础。在当代,能源同信息、材料一起构成了现代文明的三大支柱。
(1)为了降低汽车尾气对大气的污染,江苏有关部门拟用甲醇替代液化石油气作为公交车的燃料。已知:在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。请写出表示甲醇燃烧热的热化学方程式。
(2)测定工业甲醇中CH3OH的质量分数可按下法:取0.1000g工业甲醇样品,以适量H2SO4酸化后,加入20.00mL 0.2000mol/L的K2Cr2O7溶液,再用0.3000mol/L (NH4)2Fe(SO4)2标准溶液滴定,耗去此标准液20.00mL时,刚好到达滴定终点。
已知:CH3OH+Cr2O72-+8H+=CO2↑+2Cr3++6H2O
①写出H2SO4酸化的K2Cr2O7溶液与(NH4)2Fe(SO4)2溶液反应的离子方程式。
②此工业甲醇中CH3OH的质量分数为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com