
分析 (1)OH-的摩尔质量为17g/mol,根据m=nM计算其质量,OH-含有10个电子,电子物质的量为氢氧根离子的10倍,再根据N=nNA计算电子数目;
(2)根据n=$\frac{m}{M}$计算 SO2、CO、NO的物质的量之比,结合分子式计算含有氧原子数目之比,相同条件下气体体积之比等于其物质的量之比;
(3)设水的体积为1L,则HCl的体积为448L,根据n=$\frac{V}{{V}_{m}}$计算HCl物质的量,根据m=nM计算HCl质量,溶液质量=水的质量+HCl的质量,质量分数=$\frac{HCl质量}{溶液质量}$×100%,根据V=$\frac{m}{ρ}$计算溶液体积,再根据c=$\frac{n}{V}$计算物质的量浓度.
解答 解:(1)OH-的摩尔质量为17g/mol,0.4mol OH-的质量为 0.4mol×17g/mol=6.8g,OH-含有10个电子,则0.4mol OH-含有电子数目为0.4mol×10×6.02×1023mol-1=2.408×1024,
故答案为:6.8g; 2.408×1024;
(2)质量比为16:7:6的SO2、CO、NO的物质的量之比为$\frac{16g}{64g/mol}$:$\frac{7g}{28g/mol}$:$\frac{6g}{30g/mol}$=5:5:4,则含有氧原子数目之比为5×2:5×1:4×1=10:5:4,相同条件下气体体积之比等于其物质的量之比,三者体积比为5:5:4,
故答案为:10:5:4;5:5:4;
(3)设水的体积为1L,则HCl的体积为448L,标况下HCl物质的量=$\frac{448L}{22.4L/mol}$=20molHCl质量为20mol×36.5g/mol=730g,溶液质量=1L×1000g/L+730g=1730g,
溶液质量分数=$\frac{730g}{1730g}$×100%=42.2%,
溶液体积=$\frac{1730g}{1100g/L}$=$\frac{173}{110}$L,则物质的量浓度为$\frac{20mol}{\frac{173}{110}L}$=12.7mol•L-1.
故答案为:42.2%;12.7mol•L-1.
点评 本题考查了物质的量的有关计算,熟悉基本公式并灵活运用公式来分析解答,知道公式中各个物理量之间的关系,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类是具有甜味的物质 | |
| B. | 糖类是人体必需的营养素 | |
| C. | 葡萄糖是一种多羟基醛,不具有还原性 | |
| D. | 糖类是具有Cn(H2O)m通式的物质,糖也称为碳水化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
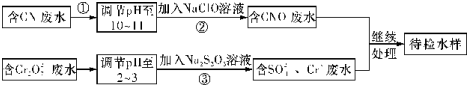
 如图是一个化学过程的示意图.请根据该示意图完成下列题目:
如图是一个化学过程的示意图.请根据该示意图完成下列题目:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
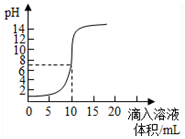
| A. | 原来盐酸的物质的量浓度为0.1mol•L-1 | |
| B. | 可以选择红色石蕊作为指示剂 | |
| C. | 氢氧化钠的物质的量浓度为0.1mol•L-1 | |
| D. | pH为7时加入的氢氧化钠的物质的量为0.1mol |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在该反应中有1 mol H2C2O4参加反应,转移电子总数为6NA | |
| B. | 该反应配平后H+的化学计量数为6 | |
| C. | 该反应右边横线上的产物为OH- | |
| D. | 该反应的氧化剂为H2C2O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
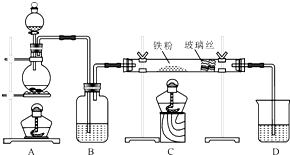 工业上,向500℃~600℃的铁屑中通入氯气生产无水氯化铁(已知炽热铁屑与氯化氢生成氯化亚铁).现用如图所示的装置模拟上述过程进行试验.
工业上,向500℃~600℃的铁屑中通入氯气生产无水氯化铁(已知炽热铁屑与氯化氢生成氯化亚铁).现用如图所示的装置模拟上述过程进行试验.查看答案和解析>>
科目:高中化学 来源: 题型:实验题

| 物质 | 颜色状态 | 密度/g/cm3 | 熔点/℃ | 沸点/℃ |
| 苯甲酸* | 白色固体 | 1.2659 | 122 | 249 |
| 苯甲酸乙酯 | 无色液体 | 1.05 | -34.6 | 212.6 |
| 乙酸 | 无色液体 | 1.0492 | 16.6 | 117.9 |
| 乙醇 | 无色液体 | 0.789 | -117.3 | 78.5 |
| 乙酸乙酯 | 无色液体 | 0.894-0.898 | -83.6 | 77.1 |
| 乙醚 | 无色液体 | 0.713 | -116.3 | 34.6 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com