
【题目】下列离子方程式正确的是( )
A.向明矾溶液中加入氢氧化钡溶液至沉淀的物质的量达到最大值:Al3++2SO ![]() +2Ba2++4OH﹣═2BaSO4↓+AlO
+2Ba2++4OH﹣═2BaSO4↓+AlO ![]() +2H2O
+2H2O
B.向澄清石灰水中通入少量CO2:OH﹣+CO2═HCO ![]()
C.醋酸溶液与水垢中的CaCO3反应:CaCO3+2CH3COOH═Ca2++2CH3COO﹣+H2O+CO2↑
D.硝酸银溶液中加入铜粉:Ag++Cu═Cu2++Ag
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源: 题型:
【题目】孔雀石的主要成分为Cu2(OH)2CO3 , 还含少量二价铁和三价铁的氧化物及硅的氧化物.如图1是实验室以孔雀石为原料制备胆矾晶体的流程图: 
请回答下列问题:
(1)溶液A中的金属离子有 . 从下列所给试剂中选择:实验步骤中试剂①为(填代号)
a、KMnO4 b、HNO3c、H2O2 d、Cl2
(2)根据图2有关数据,你认为工业上加入试剂①氧化操作时应采取的措施是:溶液温度控制在℃,pH控制在 , 氧化时间为小时左右.
(3)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,反应中MnO4﹣还原为Mn2+ , 取A溶液20.00mL,用去0.0240mol/L KMnO4溶液16.00mL时,恰好达到滴定终点,则A溶液中Fe2+浓度为mol/L.
(4)请设计一种实验方案检验溶液C中Fe3+是否完全除去(写出操作步骤、现象和结论) .
(5)由溶液C获得胆矾晶体,需要经过蒸发浓缩、、过滤等操作.除烧杯漏斗外过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是 .
(6)为测定胆矾中结晶水数目,称取24.8g硫酸铜晶体盛装在干燥的
(填仪器名称)里,灼烧至质量不再改变时,称量粉末的质量为16.0g.,则计算得胆矾(CuSO4nH2O)中n=(计算结果精确到0.1).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值.下列判断正确的是( )
A.2g H2含有的氢原子数目为NA
B.常温常压下,22.4L O2含有的分子数目为NA
C.1L 1molL﹣1 KOH溶液中含有的钾离子数目为NA
D.1mol Zn变为Zn2+时失去的电子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“盐水动力”玩具车的电池以镁片、活性炭为电极,向极板上滴加食盐水后电池便可工作,电池反应为2Mg+O2+2H2O=2Mg(OH)2 . 下列关于该电池的说法错误的是( ) 
A.镁片作为正极
B.食盐水作为电解质溶液
C.电池工作时镁片逐渐被消耗
D.电池工作时实现了化学能向电能的转化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是( )
A.中和滴定实验时,用待测液润洗锥形瓶
B.盛放NaOH溶液时,使用带玻璃塞的磨口瓶
C.用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出
D.NaCl溶液蒸发结晶时,蒸发皿中有晶体析出并剩余少量液体即停止加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中 ![]() 和
和 ![]() 代表不同元素的原子.
代表不同元素的原子. 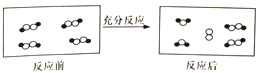
关于此反应说法错误的是( )
A.一定属于吸热反应
B.一定属于可逆反应
C.一定属于氧化还原反应
D.一定属于分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某硫酸厂产生的烧渣(主要含Fe2O3、FeO,还有一定量的SiO2)可用于制备FeCO3 , 其流程如下: 
已知:“还原”时,FeS2与H2SO4不反应,Fe3+通过反应Ⅰ、Ⅱ被还原,其中反应Ⅰ如下:
FeS2+14Fe3++8H2O=15Fe2++2SO42﹣+16H+
(1)加入FeS2还原后,检验Fe3+是否反应完全的试剂为 .
(2)所得FeCO3需充分洗涤,检验是否洗净的方法是 . “沉淀”时,pH不宜过高,否则制备的FeCO3中可能混有的杂质是 .
(3)①写出“还原”时反应Ⅱ的离子方程式: .
(4)②“还原”前后溶液中部分离子的浓度见下表(溶液体积变化或略不计):
离子 | 离子浓度(molL﹣1) | |
还原前 | 还原后 | |
Fe2+ | 0.10 | 2.5 |
SO42﹣ | 3.5 | 3.7 |
请计算反应Ⅰ、Ⅱ中被还原的Fe3+的物质的量之比(写出计算过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验能获得成功的是( )
A.用酸性高锰酸钾溶液鉴别乙烷和乙烯
B.用分液漏斗分离乙醛和水
C.用苯、溴水和铁粉混合制取溴苯
D.用紫色石蕊溶液检验苯酚弱酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含Cl﹣、SO ![]() 、和CO
、和CO ![]() ,要使每加入一种试剂(Ag+、Ba2+、H+)只去掉一种离子,操作顺序是( )
,要使每加入一种试剂(Ag+、Ba2+、H+)只去掉一种离子,操作顺序是( )
A.Ba2+→Ag+→H+
B.Ag+→Ba2+→H+
C.H+→Ba2+→Ag+
D.H+→Ag+→Ba2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com