
【题目】下列气体排放到空气中可能形成酸雨的是
A.CO2B.COC.SO2D.NH3
科目:高中化学 来源: 题型:
【题目】一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
(1)向一定物质的量浓度的Cu(NO3)2 和Mn(NO3)2 溶液中加入Na2CO3 溶液,所得沉淀经高温灼烧,可制得CuMn2O4 . ①写出基态Mn原子的价电子排布式为 .
②CO32﹣的空间构型是(用文字描述).
(2)在铜锰氧化物的催化下,CO 被氧化为CO2 , HCHO 被氧化为CO2 和H2O. ①根据等电子体原理,CO 分子的结构式为 .
②CO2 分子中C 原子轨道的杂化类型为 .
③1mol甲醛(HCHO)分子中含有的σ键数目为 .
(3)向CuSO4溶液中加入过量NH3﹒H2O溶液可生成[Cu (NH3)4]2+ . 不考虑空间构型,[Cu (NH3)4]2+的结构可用示意图表示为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究铜跟浓硫酸的反应,用下图所示装置进行有关实验。
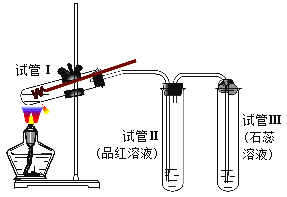
请回答下列问题:
(1)试管Ⅰ中发生反应的化学方程式为:___________________________________________。
(2)可抽动铜丝的作用是_________________________。
(3)试管Ⅱ中现象为_____________________________;可证明_____________________________________。
(4)试管Ⅲ的管口用浸有碱(NaOH溶液)的棉团塞住,其作用是___________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg-Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如下图。回答下列问题:
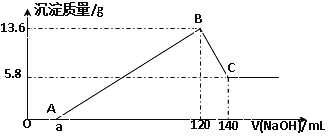
(1)写出OA段和BC段反应的离子方程式:
OA:________________________________ ; BC:_____________________________;
(2)原Mg-Al合金的质量是_____________。
(3)原HCl溶液的物质的量浓度是________________。
(4)所加NaOH溶液的物质的量浓度是____________。
(5)a的值是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下,反应2SO2+O22SO3 , 的平衡常数K=19,在该温度下的体积固定的密闭容器中充入C(SO2)=1molL﹣1 , C(O2)=1 molL﹣1 , 当反应在该温度下SO2 , 为80%时,该反应(填“是”或“否”)达到化学平衡状态,若未达到,向(填“正反应”或“逆反应”)方向进行.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】KClO3和浓盐酸在一定温度下反应,还原产物为黄绿色的易爆物二氧化氯。其变化可以表示为:![]() KClO3+
KClO3+![]() HCl(浓)―→
HCl(浓)―→![]() KCl+
KCl+![]() ClO2↑+
ClO2↑+![]() Cl2↑+
Cl2↑+![]() H2O
H2O
(1)请配平该化学方程式(未知系数填入框内)_____。
(2)浓盐酸在反应中显示出来的性质是________(填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)5 ℃ 下将产物氯气0.1 mol溶于水配成1 L溶液,已知该溶液中氢氧根离子浓度最小,请将溶液中的其他成分按照其物质的量浓度从大到小顺序排列____________________(填分子或离子化学式,少写及顺序错误不得分)。
(4)若改变温度至70 ℃,发现KClO3和浓盐酸反应的氧化产物和还原产物均为二氧化氯气体,试写出反应的化学方程式:______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com