
ŹµŃéŹŅÓŠČżĘæŹ§Č„±źĒ©µÄŹŌ¼Į£¬·Ö±šŹĒNa2CO3”¢NaCl”¢AgNO3 £¬ŹµŃéŌ±Ń”ŌńĮĖŅ»ÖÖŹŌ¼Į¾Ķ°ŃĖüĆĒĒų±šæŖĄ“ĮĖ£¬ÕāÖÖŹŌ¼ĮŹĒ£ŗ
A£®ĀČ»Æ±µČÜŅŗ B£®ĒāŃõ»ÆÄĘČÜŅŗ C£®ŃĪĖį D£®ĻõĖį
 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓėH2SO4·“Ó¦µÄĀĮ·Ū7.2g | |
| B£® | ²Ī¼Ó·“Ó¦µÄH2SO4ĪŖ0.2mol | |
| C£® | ĀĮÓėNaOH·“Ó¦ÖŠĻūŗÄŃõ»Æ¼ĮŌ¼0.53mol | |
| D£® | ²Ī¼Ó·“Ó¦µÄNaOHŌ¼ĪŖ0.27mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğŌĘÄĻŹ”øßŅ»9ŌĀŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŠšŹöÕżČ·µÄŹĒ
A£®¹ĢĢåĀČ»ÆÄĘ²»µ¼µē£¬ĖłŅŌĀČ»ÆÄĘŹĒ·Ēµē½āÖŹ B£®ĶĖæÄܵ¼µē£¬ĖłŅŌĶŹĒµē½āÖŹ
C£®ĀČ»ÆĒāĖ®ČÜŅŗÄܵ¼µē£¬ĖłŅŌĀČ»ÆĒāŹĒµē½āÖŹ D£®SO3ČÜÓŚĖ®Äܵ¼µē£¬ĖłŅŌSO3ŹĒµē½āÖŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĞĻÄĪĄŅ»øßŅ»ÉĻ10ŌĀŌĀæ¼»Æѧa¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
Ń”ŌńĻĀĮŠŹµŃé·½·Ø·ÖĄėĪļÖŹ£¬½«·ÖĄė·½·ØµÄŠņŗÅĢīŌŚŗįĻßÉĻ”£
A ŻĶČ”·ÖŅŗ B Éż»Ŗ C ½į¾§ D ·ÖŅŗ E ÕōĮó F¹żĀĖ
¢Ł_____·ÖĄė±„ŗĶŹ³ŃĪĖ®Óėɳ×ӵĻģŗĻĪļ”£
¢Ś_____“ÓĻõĖį¼ŲŗĶĀČ»ÆÄʵĻģŗĻŅŗÖŠ»ńµĆĻõĖį¼Ų”£
¢Ū______·ÖĄėĖ®ŗĶĘūÓĶµÄ»ģŗĻĪļ”£
¢Ü_____·ÖĄėCCl4(·ŠµćĪŖ76.75”ę)ŗĶ¼×±½(·ŠµćĪŖ110.6”ę)
¢Ż______·ÖĄė³ö»ģŌŚÉ³ĶĮÖŠµÄµāµ„ÖŹ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĞĻÄĪĄŅ»øßŅ»ÉĻ10ŌĀŌĀæ¼»Æѧa¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠø÷×éĪļÖŹÖŠ£¬Ėłŗ¬·Ö×ÓŹżĻąĶ¬µÄŹĒ
A£®1gH2ŗĶ1gO2 B£®5.6LN2(±ź×¼×“æö)ŗĶ22gCO2
C£®9gH2OŗĶ0.5molCl2 D£®22.4LH2(±ź×¼×“æö)ŗĶ0.1molN2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĞĻÄĪĄŅ»øßŅ»ÉĻ10ŌĀŌĀæ¼»Æѧa¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
30ml 5mol/LNaOHČÜŅŗÖŠNaOHµÄÖŹĮæĪŖ
A£®4g B£®5g C£®6g D£®7g
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğ°²»ÕŹ¦“óø½ÖŠø߶žÉĻ10ŌĀŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ņ»¶ØĢõ¼žĻĀČÜŅŗµÄĖį¼īŠŌ¶ŌTiO2¹ā“ß»ÆČ¼ĮĻR½µ½ā·“Ó¦µÄÓ°ĻģČēĶ¼ĖłŹ¾”£ĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ
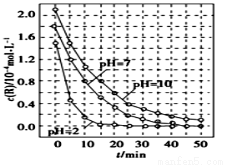
A£®ČÜŅŗĖįŠŌŌ½Ē棬R µÄ½µ½āĖŁ ĀŹŌ½Š”
ĀŹŌ½Š”
B£®RµÄĘšŹ¼ÅضČŌ½Š”£¬½µ½āĖŁĀŹŌ½“ó[
C£®ŌŚ0”«50 minÖ®¼ä£¬pH=2ŗĶPH=7Ź±RµÄ½µ½ā°Ł·ÖĀŹĻąµČ
D£®ŌŚ20”«25 minÖ®¼ä£¬pH=10 Ź±RµÄĘ½¾ł½µ½āĖŁĀŹĪŖ0.04 mol”¤L£1”¤min£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
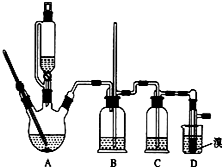 ŹµŃéŹŅÖʱø1£¬2-¶žäåŅŅĶéµÄ·“Ó¦ŌĄķČēĻĀ£ŗ
ŹµŃéŹŅÖʱø1£¬2-¶žäåŅŅĶéµÄ·“Ó¦ŌĄķČēĻĀ£ŗ| ŅŅ“¼ | 1£¬2-¶žäåŅŅĶé | ŅŅĆŃ | |
| דĢ¬ | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå | ĪŽÉ«ŅŗĢå |
| ĆܶČ/g•cm-3 | 0.79 | 2.2 | 0.71 |
| ·Šµć/”ę | 78.5 | 132 | 34.6 |
| ČŪµć/”ę | Ņ»l30 | 9 | -1l6 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com