
| A. | 如果苯酚浓溶液沾到皮肤上,应立即用自来水冲洗 | |
| B. | 受溴腐蚀致伤时,应先用苯和甘油洗伤口,再用水洗 | |
| C. | 检验氨基酸时,可向氨基酸溶液中加双缩脲试剂,会呈现紫玫瑰色 | |
| D. | 纸层析法点样时应用玻璃棒蘸取试样,在滤纸条原点处轻轻点样,晾干后再点,重复3〜5次 |
分析 A.苯酚易溶于酒精,常温下不溶于水;
B.依据溴易溶于苯、甘油;
C双缩脲试剂检验肽键;
D.纸层析法点样时不能用玻璃棒蘸取试样.
解答 解:A.如果苯酚浓溶液沾到皮肤上,应立即用酒精洗,故A错误;
B.苯、甘油都是有机溶剂,可以迅速溶解溴,使危害降到最低,所以受溴腐蚀致伤时,应先用苯和甘油洗伤口,再用水洗,故B正确;
C.蛋白质与双缩脲试剂会呈现紫玫瑰色,可以用双缩脲试剂碱液蛋白质,氨基酸不具有此性质,故C错误;
D.点样时不能用玻璃棒,应用毛细管蘸取试样在原点轻轻点样,晾干后再点,故D错误;
故选:B.
点评 本题考查了实验安全及事故处理,明确相关物质的性质及常用实验基本操作是解题关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 蛋白质溶液中加入Na2SO4可使其变性 | |
| B. | 蔗糖水解生成互为同分异构体的葡萄糖和果糖 | |
| C. | 顺-2一丁烯和反-2-丁烯的加氢产物不同 | |
| D. | 石油的分馏和煤的于馏均属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
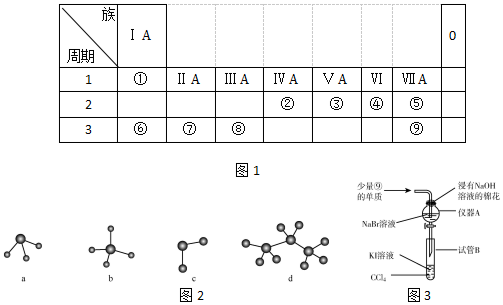
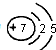 .
. →
→ ,元素⑥和⑨形成的化合物中含有离子键.
,元素⑥和⑨形成的化合物中含有离子键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体的压强 | B. | 混合气体的密度 | ||
| C. | B的物质的量浓度 | D. | 混合气体的平均相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 具有相同电子层数而又按原子序数递增顺序排列的横行称为周期 | |
| B. | 元素周期表共有14列元素:7个主族和7个副族 | |
| C. | 元素周期表的第一列元素称为第IA族,均为活泼的金属元素 | |
| D. | 元素周期表中第二周期第VIIA族元素的最高正价为+7价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成物化学键形成时也会吸收热量 | |
| B. | 生成物的总能量高于反应物的总能量 | |
| C. | 一定需要加热条件下才能实现 | |
| D. | 使用催化剂可以降低吸热反应的热效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 48 mol•(L•s )-1 | B. | 36 mol•(L•s )-1 | C. | 24 mol•(L•s )-1 | D. | 12 mol•(L•s )-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 60g丙醇中存在的共价键总数为10NA | |
| B. | 92g乙醇与足量的金属钠反应,生成氢气(H2)的分子数为NA | |
| C. | 标准状况下,22.4L已烷中碳碳键数目为5NA | |
| D. | 乙烯和甲醚的混合物共0.1mol,完全燃烧所消耗的氧分子数一定为0.6NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com