
| A.非金属性X<Y<Z | B.原子半径X>Y>Z |
| C.气态氢化物的稳定性X>Y>Z | D.原子最外层电子数X<Y<Z |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
 b
b  c
c 
 点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。
点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | | | |||||||||||||||
| | | | | ① | ⑩ | ② | ③ | | |||||||||
| | ④ | ⑤ | | | ⑦ | ⑧ | ⑨ | ||||||||||
| | | | | | | | | | | | | | | | ⑥ | | |
| | | | | | | | | | | | | | | | | | |
 ________________________________________________。
________________________________________________。
 元素⑧单质能溶于水,水液呈 色,在其中通入元素⑦的某种氧化物,溶液颜色褪去,用化学方程式表示原因 。
元素⑧单质能溶于水,水液呈 色,在其中通入元素⑦的某种氧化物,溶液颜色褪去,用化学方程式表示原因 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| Q | 只有一种能级,其电子总数等于能层序数 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:R>Q | B.R和Q可形成离子化合物 |
| C.R和Q可形成共价化合物RO | D.R和Q可形成共价化合物RO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X和Y都是非金属元素,其中X的最高化合价为+5价 |
| B.元素X可形成化学式为KXO3的盐 |
| C.X与Y所能形成的化合物都是酸性氧化物 |
| D.X的氢化物极易溶于水,可以用来做喷泉实验 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
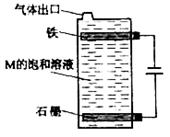
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
|
|
|
|
 D.稳定性:H2A > HC
D.稳定性:H2A > HC查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com